1��ѡ���� ij�����к���Ca2+��Mg2+��SO42�������ʣ��ֲⶨ�Ȼ��ƺ�����ȡ120g��������ˮ���˳�ȥ6g���������Һ�����μ�������������Լ���1mol/L������������Һ200 mL��4.56g�����Ȼ�����31.8%��̼������Һ10g�����ְ�ɫ���������࣬���˳�ȥ������,������Һ�м�����������ᣬʹ��Һ�����ԣ������������Ȼ��ƾ���126.65g��������к��Ȼ��Ƶ���������Ϊ
A��94.1%����
B��92.9%�� ��
C��86.3%������
D��83.2%
�ο��𰸣�B
���������������������������������ƺ��ȥþ���ӣ�ͬʱ������������Ϊ0.2mol�������Ȼ�����ȥ��������ӣ������������ӣ�����̼����0.03mol����ȥ�����ı����Ӻ����ӣ�����������0.06mol�����˺���������ȥ���������Ӻ�̼������ӣ����ɺ�������ȫ��ת��Ϊ�Ȼ��ƣ���Ϊ���������ӵ��Ȼ���Ϊ0.26mol������Ϊ15.12g��ԭ�������Ȼ���Ϊ111.53g����������Ϊ0.929����ѡB��
����������Ҫ���dz��ӹ����������µ����ʣ������������Ȼ��������м��㡣���ڽ��ۺ����⡣
�����Ѷȣ�һ��
2��ѡ���� ���м������е���
A���ð�ˮ����Al3+��Mg2+��Ag+
B���ú˴Ź���������1��������2�������
C����Ba(NO3)2��Һ����Cl����SO42-��CO32-
D����KMnO4������Һ����CH3CH��CHCH2OH��CH3CH2CH2CHO
�ο��𰸣�B
�����������ˮ��Al3+��Mg2+�����ɰ�ɫ�������ʲ����ð�ˮ����Al3+��Mg2+��A����
1�����������������ԭ�ӡ�2�����������������ԭ�ӣ��ʿ��ú˴Ź������������ߣ�B��ȷ��
Ba(NO3)2��Һ��SO42-��CO32-�����ɰ�ɫ�������ʲ�����Ba(NO3)2��Һ����SO42-��CO32-��C����
CH3CH��CHCH2OH��CH3CH2CH2CHO����ʹKMnO4������Һ��ɫ���ʲ�����KMnO4������Һ�������ߣ�D����
�����Ѷȣ�һ��
3������� ij����С���о���������Al2O3�ĺ������������ϵ�֪�����������Ҫ�ɷ���Al2O3��������Fe2O3��SiO2�ȣ�������������ȡAl2O3�Ĺ������£�
��1������B����Ҫ��;�У�д��1�����ɣ���______��
��2���ڢٲ������������м��������ռ���Һ������Ӧ�����ӷ���ʽ�ǣ�
______��
______��
�ڢ۲��У��������������Ļ�ѧ����ʽ�ǣ�______��
��3����ʵ����������ù��徫ȷ����������С�鷢�������������������������ԭ������������ȣ������������Al2O3�����������ǣ�______��������һλС����
��4����ҵ����ȡAlCl3��Al2O3��C��Cl2�ڸ��������·�Ӧ��ÿ����0.5mol̼���ʣ�ת��1mol���ӣ���Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣���1�����������м��������ռ���Һ�����ڢٵõ���Һ�к���ƫ��������ӡ���������ӣ�����Ϊ������������������Ϊ������ԭ�ϣ�������Ϊ��ɫ��������Ϳ�ϡ�����ȣ�
�ʴ�Ϊ������ԭ�ϡ�����Ϳ�ϡ�����ȣ�
��2�����ݿ�ͼ���̣����������м��������ռ���Һ�����������������������Һǿ��������ǿ�ֻFe2O3����ǿ�ᣬ�����ڼSiO2ֻ����ǿ��������ᣬ���ڢٵõ���Һ�к���ƫ��������ӡ���������ӣ�����Ϊ������������������������Һ����Ӧ��
�����������м��������ռ���Һ������Ӧ�����ӷ���ʽ��Al2O3+2OH-=2AlO2-+H2O��SiO2+2OH-=SiO32-+H2O��
����B����������A�к���ƫ�����ƺ������Լ��������������ƣ�������������������ɹ���������Ȼ�����������Ӧ�����ӷ���ʽ��SiO2+2OH-=SiO32-+H2O��
������C�ǹ��ᣬD�к����Ȼ��������ᣬ��˷�Ӧ�������������������Լ��ǰ�����ˮ�����������������ķ���ʽ��AlCl3+3NH3?H2O=Al��OH��3��+3NH4Cl��
�ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��SiO2+2OH-=SiO32-+H2O��AlCl3+3NH3?H2O=Al��OH��3��+3NH4Cl��
��3����ʵ����������ù��徫ȷ����������С�鷢�������������������������ԭ������������ȣ�˵�������������������������ԭ������������ȣ�����������Al2O3������������������������������������������ͬ�ģ�����Ϊ����������д��Al2O3?3H2O����ʽ����������������102102+54��100%=65.4%��
�ʴ�Ϊ��65.4%��
��4��Cl2��ǿ�����ԣ�̼���л�ԭ�ԣ�ÿ����0.5 mol ̼���ʣ�ת��1mol���ӣ���˵����Ӧ��̼ʧȥ2�����ӣ�������������CO�����Է�Ӧ�Ļ�ѧ����ʽ��Al2O3+3Cl2+3C����.2AlCl3+3CO��
�ʴ�Ϊ��Al2O3+3Cl2+3C����.2AlCl3+3CO��
���������
�����Ѷȣ���
4��ѡ���� Ϊ��ȥ�����������������ʣ������ڵ����ʣ����йس����Լ��Ͳ�����������
A���Ҵ���ˮ�������������ƹ��壬����
B���������������ᣩ��������������Һ����Һ
C����ˮ���廯�ƣ������ӹ������漰�IJ����У���CCl4����ȡ����Һ
D�������ᣨ�������ƣ�����ϡ���ᣬ����
�ο��𰸣�C
���������������ʷ����ᴿ����ʱ,ѡ���Լ���ʵ���������Ӧ��ѭ����ԭ��: 1.���������µ����ʣ�ˮ���⣩���������ᴿ�������Ӧ�Ǵ����������Һ�����������������ʻ������У�2.�����ᴿ�������״̬���䣻3.ʵ����̺Ͳ������������У���ѡ������ᴿ����Ӧ��ѭ��������ѧ���ȼ��ӵ�ԭ�ݴ˿��Խ��A���Ҵ���ˮ���ܣ�����Ҫ��ȥ�Ҵ���Һ�е�ˮ��Ҫ������ʯ�ң�Ȼ�����ɣ�A����ȷ��B����������Ҳ�ܺ�����������Һ��Ӧ������Ҫ��ȥ���������е����ᣬ��Ҫ���뱥��̼������Һ��Ȼ���Һ���ɣ�B����ȷ��C���������������л��ܼ��У����Ҫ��ȥ��ˮ�е��廯�ƣ�����������ȡ����˳��ӹ������漰�IJ����У���CCl4����ȡ����Һ��C��ȷ��D��Ҫ��ȥ�������еı��������йؼ���Ũ���ᣬȻ�����ɣ�D����ȷ����ѡC��
�����Ѷȣ�һ��
5������� ����ʯ����Կ�����MgO��Fe2O3��Al2O3��SiO2��ɣ�������ʯ��ȡ��ʽ̼��þ��ʵ�鲽�����£�
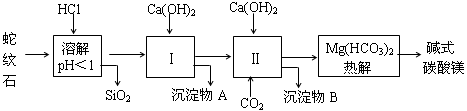
��1������ʯ��������ܽ����Һ�����Mg2+�⣬�����еĽ���������?��
��2�����Т����ʱ��������Һ��pH=7~8���й��������������pH���±�����Ca(OH)2���ܹ�������Ca(OH)2�������ܻᵼ��?�ܽ⣬����?������
��������
| Fe(OH)3
| Al(OH)3
| Mg(OH)2
|
��ʼ����pH
| 1.5
| 3.3
| 9.4
|
?
��3���ӳ��������A����ȡ��ɫ��������Ϊ���ϣ����������A�м���?����������ʵĻ�ѧʽ����Ȼ��?��������дʵ��������ƣ�������ѭ��ʹ�ã��ܽ�Լ��Դ������ʵ���У�����ѭ��ʹ�õ�������?����д���ʵĻ�ѧʽ����
��4�������ʵ�飬ȷ����ƷaMgCO3��bMg(OH)2��cH2O��a��b��c��ֵ����д������ʵ�鲽��������Ҫ�ⶨ����Ŀ�������Լ���Ũ���ᡢ��ʯ�ҡ�����������Һ������ʯ��ˮ��������Ʒ�������ڸ��·ֽ⣬��?����?����MgO������
��5��������������װ�б�Ҫ���Լ�����ѡ���������ʵ�������������������һ��װ��?��ѡ���������� �����ظ�ʹ�ã��á�A��B������������ʾ��
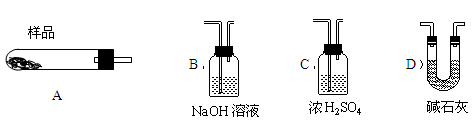
��6��18.2g��Ʒ��ȫ�ֽ����6.6gCO2��8.0gMgO���ɴ˿�֪����Ʒ�Ļ�ѧʽ��a=?��b=?��c=?��
�ο��𰸣���1��Fe3+��Al3+
��2��Al(OH)3��Mg(OH)2��
��3��NaOH�����ˡ�ϴ�ӡ����գ�CO2��
��4��������������������������̼��������
��5��A��C��D��D
��6��3? 1? 3
�����������1������ʯ����Կ���MgO��Fe2O3��Al2O3��SiO2��ɣ�����ʯ�������ܽ��MgO��Fe2O3��Al2O3��HCl��Ӧ�ܽ⣬��SiO2��HCl����Ӧ�������ܽ⡣
��2�����������ƹ���ʱ����Һ������ǿ��Al(OH)3���ܽ⣬���������������pH���пɿ�����Mg��OH��2��pHΪ9.4ʱ��ʼ���������Լ�����ǿMg(OH)2�������
��3����ɫ������ΪFe2O3��Ӧ�Ƚ����к��е�����Al(OH)3��ȥ����ȥAl(OH)3�ķ�����������������ǿ������ʣ��˹�����CO2�ǿ����ظ�ʹ�õġ�
��4��ȷ����ƷaMgCO3?bMg��OH��2?cH2O��a��b��c��ֵ����Ҫ�ⶨ�������Ǣ���Ʒ��������MgO������������CO2�����������������������ˮ��������
��5��AΪ��Ʒ��Ӧװ�ã����Ⱥ����ˮ�����Ͷ�����̼���壬Ϊ�ⶨ����������Ӧ��������Cװ�ã��ⶨˮ��������������C�������ⶨ������̼����ʱӦѡ��D������B����Һ����ˮ����C�����ױ�C���գ�������Ϊ��ֹ�����еĶ�����̼��ˮ������D���ղ�������Ӧ������������Dװ�á��ʴ�ΪA��C��D��D��
��6��m����Ʒ��=18.2g��m��CO2��=6.6g��m��MgO��=8.0g����ʽ̼��þ�ֽ⣺aMgCO3?bMg��OH��2?cH2O ��a+b��MgO+aCO2��+��b+c��H2O�������������غ�ã�m��H2O��=18.2g-6.6g-8.0g=3.6g����m��MgO���T0.2mol��n��CO2���T0.15mol��n��H2O���T0.2mol���ã�a��b��c=0.15��0.05��0.15=3��1��3��
��a+b��MgO+aCO2��+��b+c��H2O�������������غ�ã�m��H2O��=18.2g-6.6g-8.0g=3.6g����m��MgO���T0.2mol��n��CO2���T0.15mol��n��H2O���T0.2mol���ã�a��b��c=0.15��0.05��0.15=3��1��3��
�����Ѷȣ�����