1、选择题 下列关于钠的说法不正确的是
A.金属钠与O2反应,条件不同,产物不同
B.钠―钾合金通常状况下呈液态,可作原子反应堆的导热剂
C.钠的化学活泼性很强,少量的钠可保存在煤油中
D.将金属钠投入水中,生成氢氧化钠,同时放出O2
参考答案:D
本题解析:考查钠的应该性质、用途及保存等。钠是活泼的金属,极易和水生成,生成氢氧化钠和氢气,所以选项D不正确,其余都是正确的,答案选D。
本题难度:简单
2、选择题 下列有关叙述中正确的是
A.Mg和Al都可以用电解法冶炼得到
B.Na2O2、Na2O组成元素相同,与CO2反应产物也相同
C.用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3
D.Mg和Fe在一定条件下与水反应都生成H2和对应的碱
参考答案:A
本题解析:Mg和Al都是活泼的金属,都可以用电解法冶炼,A正确;虽组成元素相同,但分类不同,与CO2反应的产物不完全相同,B错;过量的KSCN溶液能与FeCl3溶液反应,但生成物不是沉淀或气体,不能除去其中的杂质,何况KSCN溶液,也引进新的杂质,C错;Fe与水蒸气反应生成的产物不是碱,而是四氧化三铁,D错。答案选A。
本题难度:简单
3、选择题 钠在干燥空气中形成的氧化物0.70g,溶于水后,可被100g质量分数为0.73%的盐酸恰好中和,钠的氧化物的成分是(?)
A.Na2O2和Na2O
B.Na2O
C.Na2O2
D.无法确定
参考答案:A
本题解析:由于不知道产物是 Na2O还是Na2O2,或者二者都有,因此设定一个化学式Na2OX,算出摩尔质量,与两种氧化物的对比即可判断。
n(盐酸)=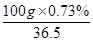 =0.02mol
=0.02mol
溶液恰好能被100g?质量分数为0.73%的盐酸溶液中和
则? Na2OX?~2NaOH~2HCl
0.01mol?0.02mol
则Na2OX平均摩尔质量M=0.70g÷0.01mol=70g/mol,介于Na2O(62g/mol)和Na2O2(78g/mOl)之间,因此,一定条件下钠与氧气反应的生成物是Na2O 和Na2O2,答案选A。
点评:该题是高考中的常见题型,属于中等难度的试题。试题在注重基础知识巩固与训练的同时,侧重对学生能力的培养和解题方法的指导与训练。解题若用极限法计算,计算比较繁琐,而用平均摩尔质量来求,则比较简单,注意方法规律的总结和积累。
本题难度:一般
4、选择题 向无色酚酞试液中逐渐投入过量的Na2O2粉末,振荡,下列有关实验现象描述错误的是
[? ]
①溶液中有气泡产生②溶液一直呈现红色③开始时,溶液出现红色,最后红色褪去④自始至终都未见红色出现
A.①②
B.②③
C.③④
D.②④
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列关于钠的叙述中正确的是(?)
A.自然界中有呈游离态的钠
B.钠原子有强还原性,钠离子有弱氧化性
C.金属钠着火时可用泡沫灭火器来灭火
D.金属钠能从熔融的TiCl4中置换出金属Ti
参考答案:BD
本题解析:钠很活泼,与空气中的O2、H2O等能直接反应,所以在自然界中只能以化合态形式存在;金属钠着火时,钠与氧气反应生成过氧化钠,泡沫灭火器是利用CO2灭火,而过氧化钠与CO2反应会生成O2(氧气助燃)。
本题难度:简单