1、选择题 在实验室中,下列除杂的方法正确的是( ?)
A.溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴
B.乙烷中混有乙烯,通H2在一定条件下反应,使乙烯转化为乙烷
C.硝基苯中混有浓H2SO4和浓HNO3,将其倒入NaOH溶液中,静置,分液
D.乙烯中混有CO2和SO2,将其通过盛有NaOH溶液的洗气瓶
参考答案:CD
本题解析:溴能把碘化钾氧化生成单质碘,碘易溶再有机溶剂中,且汽油和溴苯是易溶的,A不正确,应该用氢氧化钠溶液。B不正确,这样容易引入杂质氢气,应该是通过溴水。所以正确的答案选CD。
本题难度:简单
2、实验题 (10分)“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯。完成下列问题:
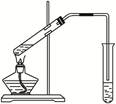
(1)写出制取乙酸乙酯的化学反应方程式__________________________________________。
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:________________。
(3)浓硫酸的作用是:①___________________________;②___________________________。
(4)饱和碳酸钠溶液的主要作用是
__________________________________________________。
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止
___________________________________________。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是____________________________。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是
______________________________________________________________________________。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) _________________。
①单位时间里,生成1 mol乙酸乙酯,同时生成1 mol水
②单位时间里,生成1 mol乙酸乙酯,同时生成1 mol乙酸
③单位时间里,消耗1 mol乙醇,同时消耗1 mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化
参考答案:
(1)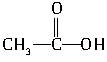 +CH3―CH2―OH
+CH3―CH2―OH
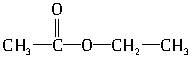 +H2O
+H2O
(2)先在试管中加入一定量的乙醇,然后边加边振荡试管,将浓硫酸慢慢加入试管,最后再加入乙酸
(3)催化作用?吸水作用
(4)中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味,溶解挥发出来的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯
(5)倒吸
(6)分液
(7)防止大试管中液体暴沸而冲出导管
(8)②④⑤
本题解析:该题是将乙酸乙酯的制取实验和无机化学的化学平衡有机结合起来的一道综合题。它涉及乙酸乙酯制取的各个环节,都是最基本的知识,而平衡状态的判断也是基础性的,根据平衡移动原理很容易进行判断。
本题难度:简单
3、实验题 请完成有关氨气的问题。
(1)实验室常用下列装置和选用的试剂制取NH3,其中正确的是__________(填序号)。

(2)若实验室收集NH3要采用法__________。
(3)若检验NH3,可用__________。
参考答案:(1)B、D
(2)向下排空气
(3)湿润的红色石蕊试纸变蓝(或用蘸取浓盐酸的玻璃棒,接近容器口,将产生大量的白烟)
本题解析:(1)C装置不对,试管口应略低于试管底部,A装置在试管口部位又生成NH4Cl得不到NH3。(2)NH3易溶于水且比空气轻。(3)利用NH3・H3O易分解生成NH3的性质。
本题难度:简单
4、选择题 实验室利用下列各组物质制备和收集气体,能采用下图装置的是
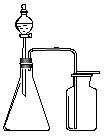
A.用熟石灰和氯化铵加热反应制NH3
B.铜与稀硝酸反应制NO
C.过氧化氢与二氧化锰混合制O2
D.用金属锌与稀硫酸反应制H2
参考答案:C
本题解析:略
本题难度:简单
5、实验题 硫酸亚铁铵的化学式为(NH4)2SO4・FeSO4・6H2O,商品名为莫尔盐。可由硫酸亚铁与硫酸铵反应生成硫酸亚铁铵,一般硫酸亚铁盐在空气中易被氧化,而形成莫尔盐后就比较稳定了。三种盐的溶解度(单位为g/100g水)如下表:
温度/℃
| 10
| 20
| 30
| 40
| 50
| 70
|
(NH4)2SO4
| 73.0
| 75.4
| 78.0
| 81.0
| 84.5
| 91.9
|
FeSO4・7H2O
| 40.0
| 48.0
| 60.0
| 73.3
| -
| -
|
(NH4)2SO4?FeSO4?6H2O
| 17.2
| 26.4
| 33.0
| 46.0
| ―
| ―
|
(一)?实验室制取少量莫尔盐的流程如下:

试回答下列问题:
(1)步骤1中加入10%Na2CO3溶液的主要作用是除去铁屑表面的油污,简述其除去油污的原理?
(2)将(NH4)2SO4与FeSO4混合后加热、浓缩,停止加热的时机?
(3)步骤4中析出的晶体不含(NH4)2SO4和FeSO4的原因是?,理论上制得的莫尔盐的质量为?。
(二)称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液。用未知浓度的KMnO4酸性溶液进行滴定。
(1)滴定时,将KMnO4酸性溶液装在_______(填“酸式”或“碱式”)滴定管。试写出该滴定过程中的离子方程式:___?__;
(2)判断该反应到达滴定终点的现象为?;
(3)假设到达滴定终点时,用去V mL KMnO4酸性溶液,则该KMnO4酸性溶液的浓度为?mol/L
参考答案:(一)(1)热的Na2CO3会发生水解反应使溶液碱性,在碱性条件下使油脂充分水解而除去(2) ?浓缩至液体表面出现洁净薄膜(3) 在相同温度下,(NH4)2SO4・FeSO4・6H2O的溶解度比(NH4)2SO4、FeSO4小;7(m1―m2)g
(二).(1)酸式? 5Fe2+ + MnO4- + 8H+= 5Fe3++ Mn2+ + 4H2O(2)当最后一滴KMnO4酸性溶液滴下时,溶液变成紫色,30s内不褪色,说明达到滴定终点(3)1/V
本题解析:
本题考查莫尔盐的制备。(一)(1)Na2CO3会发生水解反应使溶液碱性,碱性条件下酯类物质发生水解反应;(2)蒸发时不能将水蒸干,因为Fe2+容易被氧化;(3)通过比较表格中数据发现,在相同温度下,(NH4)2SO4・FeSO4・6H2O的溶解度比(NH4)2SO4、FeSO4小,所以析出的是(NH4)2SO4・FeSO4・6H2O,参加反应铁的质量为(m1―m2)g,根据铁元素的守恒:Fe~(NH4)2SO4・FeSO4・6H2O,求出莫尔盐的质量为:7(m1―m2)g;(二)(1)KMnO4酸性溶液具有强氧化性,能够氧化橡胶管,应该用酸式滴定管盛装;(2)Fe2+被氧化为Fe3+,MnO4-被还原成Mn2+,则滴定终点时,紫色变为无色,若30s内不褪色,说明达到滴定终点;(3)依据关系式:5Fe2+~MnO4-,1.96g的该硫酸亚铁铵的物质的量为0.005mol,则n(Fe2+)=0.005mol,所以求出n(MnO4-)=0.001mol,c(MnO4-)="1/V" mol/L。
本题难度:一般