1、选择题 25℃时,浓度均为0.2 mol・L-1的NaHCO3和Na2CO3溶液中,下列判断正确的是?
[? ]
A.后者仅存在着水解平衡,不存在着电离平衡
B.两溶液中存在的粒子种类相同
C.c(OH-)前者大于后者
D.分别加入NaOH固体,恢复到原温度,c(CO32-)前者增大后者减小
2、简答题 结合如图所示的实验装置(铁架台等辅助仪器略去未画)
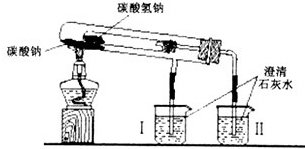
回答下列问题:
(1)在加热过程中能观察到产生白色沉淀的烧杯是______(填“Ⅰ”、“Ⅱ”)烧杯.该烧杯中发生反应的离子方程式是:______,通过实验甲可比较出Na2CO3、NaHCO3两种固体,______更稳定.
(2)若某Na2CO3固体中混有少量NaHCO3杂质,除去杂质的方法为______;若某NaHCO3溶液中混有少量Na2CO3杂质,除去杂质的化学方程式为______.
3、选择题 下列关于Na2CO3和NaHCO3的说法中,正确的是
[? ]
A.在相同条件下,NaHCO3的溶解度比Na2CO3大
B.它们的水溶液都显中性
C.NaHCO3比Na2CO3稳定
D.等物质的量的Na2CO3和NaHCO3与足量的盐酸反应,放出气体的物质的量之比为1:1
4、选择题 下列关于NaHCO3的叙述,不正确的是
[? ]
A.它是一种白色粉末,溶解度大于Na2CO3 ?
B.加热至200℃左右,可完全分解,利用这种性质,可由NaHCO3制取纯碱
C.与Na2CO3相似,当质量相同,分别跟足量盐酸反应后,NaHCO3可得到较多的二氧化碳
D.其分子为NaHCO3・10H2O在空气中会风化
5、选择题 为确证NaHCO3固体中是否含Na2CO3,下列实验操作及判断正确的是
[? ]
A.观察加热时能否放出气体
B.观察加盐酸时能否放出气体
C.溶于水中,加入澄清石灰水,观察是否有白色沉淀生成
D.溶于水中,滴加少量BaCl2溶液,观察是否有白色沉淀生成