1、选择题 设nA为阿伏伽德罗常数的值,下列说法正确的是
A.2.24L NO2含有氧原子数为0.2nA
B.常温常压下,乙烯和环丙烷(C3H6)组成的28 g混合气体中含氢原子4nA
C.1molC2H6分子中含有极性键为7nA
D.pH=13的NaOH溶液中含有的OH-0.1nA
参考答案:B
本题解析:A项:没给特定的条件(温度、压强),无法确定Vm的值,不能计算,故A错。C项:C2H6的分子结构为: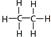 ,含有6个极性键、1个非极性键,故C错。D项:没给温度,无法确定Kw的值,不能计算,故D错。故选B。
,含有6个极性键、1个非极性键,故C错。D项:没给温度,无法确定Kw的值,不能计算,故D错。故选B。
点评:熟悉NA、物质的量、物质的量浓度、气体体积、PH之间的计算关系是解决此类问题的关键。
本题难度:简单
2、选择题 设阿伏加德较常数的数值为NA,下列说法正确的是?(?)
A.1.8g NH4+含有的电子数为NA
B.1 mol Cl2与足量Fe反应,转移的电子数为3NA
C.46g的NO2与46g的N2O4含有的原子数不同
D.标准状况下11.2L苯完全燃烧产生二氧化碳分子数为3NA
参考答案:A
本题解析:略
本题难度:简单
3、选择题 NA为阿伏加德罗常数,下列正确的是……( )
A.80g硝铵含有氮原子数为2NA
B.1L1mol・L-1的盐酸溶液中,所含氯化氢分子数为NA
C.标准状况下,11.2L四氯化碳所含分子数为0.5NA
D.在铜与硫的反应中,1mol铜失去的电子数为2NA
参考答案:A
本题解析:NA个微粒即为1mol。
A、硝铵的摩尔质量为80g・mol-1,则80g硝铵为1mol,其中所含N原子为2NA;
B、盐酸溶液中的氯化氢完全电离,无HCl分子;
C、标准状况下,CCl4为液体,因此11.2L的物质的量不是0.5mol;
D、根据2Cu+S=Cu2S,在反应中1mol铜所失电子数为1mol.
本题难度:一般
4、选择题 用NA表示阿伏加德罗常数,对生活中常见的物质下列说法中正确的是( )。
A.含有1 mol Na2CO3溶液含有的CO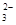 数为NA
数为NA
B.将58.5 g NaCl溶于1.00 L水中,所得NaCl溶液的浓度为1.00 mol・ L-1
C.1 mol 蔗糖(C12H22O11)在浓硫酸作用下完全脱水,转移的电子数为12NA
D.常温下,10 L pH=6的醋中含有的H+离子数为10-5NA
参考答案:D
本题解析:A.含有1 mol Na2CO3溶液,因CO 的水解,含有的CO
的水解,含有的CO 数为少于NA;B.将58.5 g NaCl溶于1.00 L水中,因为溶液的体积不是1.00mL,所得NaCl溶液的浓度不是1.00 mol・ L-1;C.蔗糖可以看做是C12(H2O)11,碳元素的平均化合价为0,故蔗糖在浓硫酸作用下完全脱水,不发生电子转移。? D.常温下,10 L pH=6的醋c(H+)=10-6mol・mol-1,故含有的H+离子数为10×10-6mol=10-5NA,正确。A为阿伏加德罗常数的值来表示微粒数目。
数为少于NA;B.将58.5 g NaCl溶于1.00 L水中,因为溶液的体积不是1.00mL,所得NaCl溶液的浓度不是1.00 mol・ L-1;C.蔗糖可以看做是C12(H2O)11,碳元素的平均化合价为0,故蔗糖在浓硫酸作用下完全脱水,不发生电子转移。? D.常温下,10 L pH=6的醋c(H+)=10-6mol・mol-1,故含有的H+离子数为10×10-6mol=10-5NA,正确。A为阿伏加德罗常数的值来表示微粒数目。
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的数值,下列说法正确的是
[? ]
A.常温常压下,1mol氦气含有的核外电子数为4NA
B.1mol的1H37Cl分子所含中子数为18NA
C.同温同压同体积的氢气和氧气有相同的分子数
D.常温时1L 1mol/L的醋酸溶液中,所含醋酸分子数为NA
参考答案:C
本题解析:
本题难度:简单