1、选择题 已知:①CO(g)+H2O(g) CO2(g)+H2(g);△H1=-41.2kJ・mol-1
CO2(g)+H2(g);△H1=-41.2kJ・mol-1
②CH4(g)+CO2(g) 2CO(g)+2H2(g);△H2=+247.3kJ・mol-1
2CO(g)+2H2(g);△H2=+247.3kJ・mol-1
③CH4(g)+H2O(g)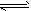 CO(g)+3H2(g);△H3
CO(g)+3H2(g);△H3
若反应③在1升的密闭容器中进行,测得CH4的物质的量浓度随反应时间的变化如图所示。下列有关叙述错误的是
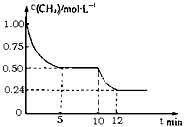
[? ]
A.△H3=+206.1 kJ・mol-1
B.反应③进行到10min时,改变的外界条件可能是升高温度
C.反应③进行的过程中,0~5min这段时间共吸收的热量为103.05kJ
D.当反应③平衡后,向容器中通入CH4,平衡向正反应方向移动,CH4的转化率将增大
2、填空题 联氨(N2H4)及其衍生物是一类重要的火箭燃料,N2H2与N2O4反应能放出大量的热。
(1)已知:2NO2(g)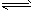 N2O4(g) ΔH=-57.20 KJ・mol-1。在一定温度下,等容密闭容器中反应达到平衡。其它条件不变时,下列措施能提高NO2转化率的是_______
N2O4(g) ΔH=-57.20 KJ・mol-1。在一定温度下,等容密闭容器中反应达到平衡。其它条件不变时,下列措施能提高NO2转化率的是_______
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)已知在T℃,2L密闭容器中,加入4mol NO2(g),发现5分钟末反应达平衡时,放出的热量为
57.20kJ,则此时N2O4的体积分数为_________,在此时间内用N2O4表示的反应速率为____________达平衡后,保持温度不变,快速缩小容器的体积至1 L,气体的颜色变化过程是_____________
(3)25℃时,1.00g N2H4(1)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量。则反应2N2H4(l)+N2O4(l)==3N2(g)+4H2O(l)的ΔH= ________________ kJ・mol-1。
(4)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300 mol・L-1、
c(N2O4)=0.0120 mol・L-1。反应2NO2(g)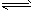 N2O4(g)的平衡常数K=___________
N2O4(g)的平衡常数K=___________
(5)T℃、1.01×105Pa,已知K=1/3,在2L密闭容器中,加入10mol NO2(g) 和4mol N2O4(g),则平衡向生成___________物质的方向移动,再次平衡时,NO2(g)的浓度是_________。
3、选择题 一定条件下,在可变容积的密闭容器中进行下列可逆反应:

下列说法正确的是
[? ]
A.达到平衡时,抽出少量氯气,反应混合液颜色变深
B.单位时间内生成2n mol S2Cl2,同时生成n mol SCl2时,平衡向逆反应方向移动
C.达平衡时,降低温度,混合液的颜色将变浅
D.单位时间内有n mol Cl2被还原,同时氧化生成n mol Cl2时,平衡向正反应方向移动
4、选择题 可逆反应aA(g)+bB(s)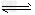 cC(g)+dD(g).在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是
cC(g)+dD(g).在反应过程中,其他条件不变,C的物质的量分数和T或P关系如图所示,下列叙述中正确的是

[? ]
A.温度降低,化学平衡向逆反应方向移动?
B.使用催化剂,C的物质的量分数增加
C.化学方程式系数a<c+d
D.无法根据图像确定改变温度后化学平衡移动方向
5、选择题 不能使2NO2(g)?N2O4(g)平衡体系中NO2与N2O4浓度的比值减小的措施是( )
A.温度、体积不变,通入NO2
B.温度、体积不变,通入N2O4
C.温度、体积不变,充入氮气
D.温度不变,缩小容器体积