1ЎўМоҝХМв ИзНјКЗТ»ёц»ҜС§№эіМөДКҫТвНјЈ®ТСЦӘјЧіШөДЧЬ·ҙУҰКҪОӘЈә2CH3OH+3O2+4KOHЁT2K2CO3+6H2O
ЈЁ1Ј©јЧіШКЗ______Ч°ЦГЈ¬НЁИлCH3OHөДөзј«ГыіЖКЗ______Ј¬Bөзј«өДГыіЖКЗ______Ј®
ЈЁ2Ј©НЁO2Т»ј«өДөзј«·ҙУҰКҪОӘ______Ј®
ЈЁ3Ј©ТТіШЦРЧЬ·ҙУҰөД»ҜС§·ҪіМКҪОӘ______Ј®
ЈЁ4Ј©өұТТіШЦРAЈЁFeЈ©ј«өДЦКБҝФцјУ6.4gКұЈ¬јЧіШЦРПыәДO2______mLЈЁұкҝцПВЈ©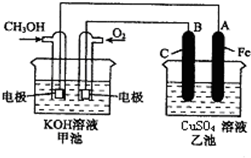
ІОҝјҙр°ёЈәЈЁ1Ј©ёщҫЭ·ҙУҰ·ҪіМКҪЦӘЈ¬јЧЧ°ЦГКЗТ»ёцИјБПөзіШЈ¬ЛщТФјЧКЗ°С»ҜС§ДЬЧӘұдОӘөзДЬөДЧ°ЦГЈ¬КЗФӯөзіШЈ»ТТУРНвјУөзФҙЈ¬ЛщТФКЗөзҪвіШЈ®ёщҫЭ2CH3OH+3O2+4KOH=2K2CO3+6H2OЦӘЈ¬CH3OH·ўЙъСх»Ҝ·ҙУҰЈ¬ЛщТФёГөзј«КЗёәј«Ј¬O2 ·ўЙъ»№Фӯ·ҙУҰЈ¬ЛщТФёГөзј«КЗХэј«Ј»КҜД«УлФӯөзіШөДХэј«ПаБ¬Ј¬ЛщТФКҜД«өзј«BКЗСфј«Ј»
№Кҙр°ёОӘЈәФӯөзіШЈ»ёәј«Ј»Сфј«Ј»
ЈЁ2Ј©ёщҫЭ2CH3OH+3O2+4KOH=2K2CO3+6H2OЦӘЈ¬CH3OH·ўЙъСх»Ҝ·ҙУҰЈ¬ЛщТФёГөзј«КЗёәј«Ј¬O2 өГөзЧУәНЛ®·ҙУҰЙъіЙЗвСхёщАлЧУЈ¬·ўЙъ»№Фӯ·ҙУҰЈ¬ЛщТФёГөзј«КЗХэј«Ј»
№Кҙр°ёОӘЈәO2+2H2O+4e-=4OH-Ј»
ЈЁ3Ј©ТТіШЦРАлЧУ·ЕөзЛіРтОӘЈәСфАлЧУ Cu2+ЈҫH+Ј¬ТхАлЧУOH-ЈҫSO42-Ј¬ТАҫЭСх»Ҝ»№Фӯ·ҙУҰөДөзЧУКШәгЈ¬ҪбәП·ҙУҰөДОпЦККйРҙ»ҜС§·ҪіМКҪЈә2CuSO4+2H2O?НЁөз?.?2CuЎэ+O2Ўь+2H2SO4
№Кҙр°ёОӘЈә2CuSO4+2H2O?НЁөз?.?2CuЎэ+O2Ўь+2H2SO4Ј»
ЈЁ4Ј©ёщҫЭөГК§өзЧУКэПаөИЈ¬СхЖшУлТшөД№ШПөКҪОӘЈә
O2--------2Cu
22.4L? ЈЁ 2ЎБ64 Ј©g
1.12L?6.40g
№Кҙр°ёОӘЈә1120Ј®
ұҫМвҪвОцЈә
ұҫМвДС¶ИЈәјтөҘ
2ЎўјЖЛгМв ЈЁ6·ЦЈ©Иф¶ЁТеДіОпЦКөДЧӘ»ҜВКОӘПыәДөфөДёГОпЦКөДОпЦКөДБҝХјЖрКјКұёГОпЦКөДФӯОпЦКөДБҝөД°Щ·ЦұИЎЈТСЦӘәПіЙ°ұ·ҙУҰОӘN2(g) + 3H2(g)  ?2NH3(g).ФЪТ»Ме»эОӘ10LЗТИЭ»эІ»ұдөДГЬұХИЭЖчЦР·ЕИл1mol N2әН3mol H2 ,ФЪТ»¶ЁМхјюПВ·ўЙъ·ҙУҰЈ¬ҫӯ4minҙпөҪ»ҜС§ЖҪәвЧҙМ¬Ј¬ІвөГИЭЖчЦР°ұЖшөДОпЦКөДБҝОӘ0.6mol.ЎЈЗуЈә
?2NH3(g).ФЪТ»Ме»эОӘ10LЗТИЭ»эІ»ұдөДГЬұХИЭЖчЦР·ЕИл1mol N2әН3mol H2 ,ФЪТ»¶ЁМхјюПВ·ўЙъ·ҙУҰЈ¬ҫӯ4minҙпөҪ»ҜС§ЖҪәвЧҙМ¬Ј¬ІвөГИЭЖчЦР°ұЖшөДОпЦКөДБҝОӘ0.6mol.ЎЈЗуЈә
ЈЁ1Ј©өӘЖшөДЧӘ»ҜВК
ЈЁ2Ј©УГЗвЖшұнКҫЖҪҫщ·ҙУҰЛЩВККЗ¶аЙЩЈҝ
ЈЁ3Ј©ЖҪәвЧҙМ¬КұЗвЖшөДОпЦКөДБҝЕЁ¶ИЎЈ
ІОҝјҙр°ёЈә
ЈЁ1Ј©30%?ЈЁ2Ј©0.0225 molЎӨ(LЎӨmin)-1?ЈЁ3Ј©0.21 molЎӨL-
ұҫМвҪвОцЈәВФ
ұҫМвДС¶ИЈәјтөҘ
3ЎўМоҝХМв АыУГПВБР·ҙУҰЈәFe+2Fe3+=3Fe2+ЙијЖТ»ёцФӯөзіШЈ¬ЗлСЎФсККөұөДІДБПәНКФјБЈ®
ЈЁ1Ј©ЗлРҙіцДгСЎУГөДХэј«ІДБПЎўёәј«ІДБПЎўөзҪвЦКИЬТәЈЁРҙ»ҜС§КҪЈ©Јәёәј«ОӘ______Ј¬Хэј«ОӘ______Ј¬өзҪвЦКИЬТәЈә______Ј®
ЈЁ2Ј©ёәј«·ҙУҰКҪЈә______Ј»Хэј«·ҙУҰКҪЈә______Ј®
ЈЁ3Ј©ИЬТәЦРFe3+Пт______ј«ТЖ¶ҜЈ¬өзЧУҙУ______ј«БчПт______ј«Ј®
ІОҝјҙр°ёЈәЈЁ1Ј©ФЪFe+2Fe3+=3Fe2+·ҙУҰЦРЈ¬Feұ»Сх»ҜЈ¬УҰОӘФӯөзіШөДёәј«Ј¬өзҪв·ҙУҰОӘЈәFe-2e-=Fe2+Ј¬Fe3+өГөзЧУұ»»№ФӯЈ¬УҰОӘФӯөзіШХэј«·ҙУҰЈ¬Хэј«ІДБПОӘ»оЖГРФұИFeөДҪрКф»т·ЗҪрКфІДБПИзМј°фЈ¬өзҪвЦКИЬТәОӘә¬Fe3+АлЧУөДИЬТәЈ¬ИзFeCl3Ј¬
№Кҙр°ёОӘЈәFeЈ»Мј°фЈ»FeCl3Ј»
ЈЁ2Ј©УЙЈЁ1Ј©ҪвҙрҝЙЦӘЈ¬ёәј«·ҙУҰОӘFe-2e-=Fe2+Ј¬Хэј«·ҙУҰОӘFe3++e-=Fe2+Ј¬№Кҙр°ёОӘЈәFe-2e-=Fe2+Ј»Fe3++e-=Fe2+Ј»
ЈЁ3Ј©ФӯөзіШ№ӨЧчКұЈ¬өзЧУҙУёәј«ҫӯНвөзВ·БчПтХэј«Ј¬ИЬТәЦРСфАлЧУПтХэј«ТЖ¶ҜЈ¬ТхАлЧУПтёәј«ТЖ¶ҜЈ¬ТФРОіЙұХәП»ШВ·Ј¬
№Кҙр°ёОӘЈәХэЈ»ёәЈ»ХэЈ®
ұҫМвҪвОцЈә
ұҫМвДС¶ИЈәТ»°г
4ЎўјтҙрМв УЙМј°фЎўМъЖ¬әН200mLПЎH2SO4ЈЁЧгБҝЈ©ЧйіЙөДФӯөзіШЦРЈ¬өұФЪМј°фЙП№І·Еіц3.36LЈЁұкЧјЧҙҝцЈ©ЖшМеКұЈ¬ЗуПыәДМъ¶аЙЩҝЛЈҝУР¶аЙЩёцөзЧУНЁ№эБЛөјПЯЈҝ
ІОҝјҙр°ёЈәЙиРиТӘПыәДМъxЈ®
ёГФӯөзіШөДөзіШ·ҙУҰКҪОӘЈә
? Fe+H2SO4=FeSO4+H2Ўь
? 56g? 22.4L
? x?3.36L
ЛщТФx=56g?ЎБ?3.36L22.4L=8.4g
јҙПыәДМъ8.4gЈ®
ЙиЧӘТЖөзЧУyЈ®
?Fe+H2SO4=FeSO4+H2Ўь ЧӘТЖөзЧУ
?22.4L? 1.204ЎБ1023ёц
?3.36L? y
ЛщТФyЁT3.36LЎБ1.204ЎБ1023ёц22.4L?=1.806ЎБ1023ёц
№Кҙр°ёОӘЈә8.4gЈ»1.806ЎБ1023ёцЈ®
ұҫМвҪвОцЈә
ұҫМвДС¶ИЈәТ»°г
5ЎўМоҝХМв ЈЁ8·ЦЈ©ПВНјКЗМҪҫҝІ»Н¬МхјюПВ»ҜС§ДЬЧӘұдОӘөзДЬөДЧ°ЦГЎЈЗл»ШҙрПВБРОКМвЈә
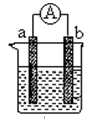
ЈЁ1Ј©өұөзј«aОӘAlЎўөзј«bОӘCuЎўөзҪвЦКИЬТәОӘПЎБтЛбКұЈ¬ёәј«өДөзј«·ҙУҰКҪОӘЈә ЎЈИз№ыТ»өзј«ЦКБҝјхЗб5.4 gЈ¬ФтБнТ»ј«·ЕіцЖшМеөДМе»эОӘ LЈЁұкЧјЧҙҝцЈ©ЎЈ
ЈЁ2Ј©ИјБПөзіШөД№ӨЧчФӯАнКЗҪ«ИјБПәНСх»ҜјБ(ИзO2)·ҙУҰЛщ·ЕіцөД»ҜС§ДЬЦұҪУЧӘ»ҜОӘөзДЬЎЈПЦЙијЖТ»ИјБПөзіШЈ¬ТФөзј«aОӘХэј«Ј¬өзј«bОӘёәј«Ј¬ЗвЖшОӘИјБПЈ¬ІЙУГKOHИЬТәОӘөзҪвТәЈ»ФтЗвЖшУҰНЁИл ј«ЈЁМоa »тbЈ¬ПВН¬Ј©Ј¬өзЧУҙУ ј«БчіцЎЈ
a ј«·ўЙъөзј«·ҙУҰКҪОӘЈә_____________________________ЎЈ
ІОҝјҙр°ёЈәЈЁ1Ј©Al-3e-= Al3+ЈЁ2·ЦЈ© 6.72 LЈЁ2·ЦЈ©
(2) ЈЁ2Ј©b b ЈЁ№І2·ЦЈ¬ёч1·ЦЈ© O2+2H2O+4e-=4OH- ЈЁ2·ЦЈ©
ұҫМвҪвОцЈәAl---H2SO4-----CuөДФӯөзіШЦРВБЧцёәј«Al-3e-= Al3+Ј¬НӯЧцХэј«2H++2 e-=H2Ј¬
ИјБПөзіШЦР»№ФӯјБОӘёәј«Ј¬Сх»ҜјБОӘХэј«Ј¬ЗвЖшОӘёәј«Ј¬өзЧУҙУёәј«БчөҪХэј«ЎЈЈЁ+Ј©O2+2H2O+4e-=4OH-
ұҫМвДС¶ИЈәТ»°г