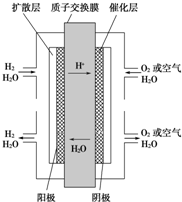
1������� ��5�֣���������������ɴ���ʹ�õ�����ȼ�ϵ����һ�����͵Ļ�ѧ��أ��乹����ͼ��ʾ�������缫���ɶ����̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ硣
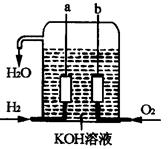
a����?����b����?����
������ӦʽΪ��?��
�ο��𰸣�����1�֣�?����1�֣�?H2 - 2e- + 2OH- =" 2" H2O��3�֣�
�����������
�����Ѷȣ���
2��ѡ���� ����п�̵�ص��ܷ�Ӧ�ǣ�Zn + 2MnO2 + 2H2O =" 2MnOOH" + Zn(OH)2���������KOH������˵����ȷ����
A��MnO2������������Ӧ
B��MnOOH��MnԪ�صĻ��ϼ�Ϊ+3
C����Ӧ���� 0.65gZn����0.01 mol���ӷ���ת��
D����������ķ�ӦΪ��Zn + 2 OH���C2e��===Zn(OH)2
�ο��𰸣�B
������������ݷ�Ӧǰ��Ļ��ϼ۱仯��֪�������������̵Ļ��ϼ��ɣ�4�۽��͵���3�ۣ����Զ�����������������������ԭ��Ӧ��A����ȷ��п�ǻ�ԭ����������������������Ӧ��1molпʧȥ2mol���ӣ�C��D����ȷ�����Դ�ѡB��
�����Ѷȣ���
3��ѡ���� Ǧ���ص������ֱ�ΪPb��PbO2,���ҺΪ����,����ʱ�ķ�ӦΪPb+PbO2+2H2SO4=2PbSO4+2H2O,���������ȷ����(? )��
A��Pb����,������
B����Һ��pH���ϼ�С
C��S ֻ��PbO2���ƶ�
ֻ��PbO2���ƶ�
D�����Һ�ܶȲ��ϼ�С
�ο��𰸣�D
���������������ѧ��Ӧ��֪,��Ӧ��Pbʧȥ����,��������PbO2�õ���,������,��Ӧ������������,��Һ��pH������������Pb����PbO2���ն�����PbSO4,����S ����PbҲ��PbO2���ƶ���PbSO4�ڵ��Һ�е��ܽ�Ⱥ�С,���Ե��Һ���ܶȲ��ϼ�С,ѡD��
����PbҲ��PbO2���ƶ���PbSO4�ڵ��Һ�е��ܽ�Ⱥ�С,���Ե��Һ���ܶȲ��ϼ�С,ѡD��
�����Ѷȣ�һ��
4��ѡ���� ��ͼΪͭ��п��ϡ����ԭ���ʾ��ͼ������˵����ȷ����
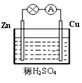
A��������ͭƬͨ����������пƬ
B��п�õ��ӣ�����ԭ
C��пΪ������ͭΪ����
D����װ���ܽ�����ת��Ϊ��ѧ��
�ο��𰸣�C
�������������ԭ��ص�Ӧ�ü��й��жϡ���ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������������õ����ӣ�������ԭ��Ӧ��п��ͭ���ã�����п�Ǹ�����ͭ����������Һ�е������ӵõ����ӣ�����������ԭ����ǰѻ�ѧ��ת��Ϊ���ܵ�װ�ã�������ȷ�Ĵ���C��
�����Ѷȣ���
5��ѡ���� Ŀǰһ�����͵ĵ��--���ӽ���Ĥȼ�ϵ�ر����������������乤��ԭ����ͼ��ʾ������������ȷ���ǣ�������
A��ͨ�������ĵ缫����������Ӧ
B��ͨ�������ĵ缫Ϊ����
C���ܷ�Ӧʽ��O2+2H2
2H2O
D�������ĵ缫��ӦʽΪO2+4H++4e-��2H2O