1、选择题 由等电子原理可推知O3、NO2-的说法中正确的是
[? ]
A.都是直线型分子
B.都是V型分子
C.都是极性分子
D.都是非极性分子
参考答案:BC
本题解析:
本题难度:一般
2、选择题 下列各组微粒中不属于等电子体的是( ? )
A.CH4、NH4+
B.H2S、HCl
C.CO2、N2O
D.CO32-、NO3-
参考答案:B
本题解析:
本题难度:一般
3、选择题 根据等电子原理,下列分子或离子与SO42-有相似结构的是
[? ]
A.PCl5
B.NF3
C.CCl4
D.N2
参考答案:C
本题解析:
本题难度:简单
4、选择题 下列分子或离子属等电子体的是( )
A.CH4和NH3
B.NO3-和CO32-
C.H3O+和PCl3
D.CS2和SO2
参考答案:B
本题解析:
本题难度:一般
5、填空题 砷化镓(GaAs)属于第三代半导体,用它制造的灯泡寿命是普通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。砷化镓的晶胞结构如下图。
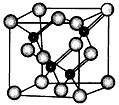
试回答:
(1)As的核外电子排布式为_____________。
(2)砷化镓晶胞中所包含的Ga原子个数为_____________。
(3)下列说法正确的是__________(填字母)。
A.砷化镓晶胞结构与NaCl相同
B.第一电离能:As> Ca
C.电负性:As> Ga
D.砷化镓晶体中含有配位键
E.半导体GaP与CaAs互为等电子体
(4)砷化镓是将(CH3)3Ga和AsH3用MOCVD方法在700℃ 时制备得到。AsH3的空间形状为____,(CH3)3Ga中镓原子的杂化方式为_____________。
(5) AsH3沸点比NH3低,其主要原因是__________________
参考答案:(1)1s22s22p63s23p63d104s24p3或[Ar]3d104s24p3
(2)4
(3)BCDE
(4)三角锥形;sp2
(5)NH3分子间能形成氢键,而AsH3分子间不能形成氢键
本题解析:
本题难度:一般