1��ѡ���� �����ڷ�����ᴿ���ʵ���ѧ������
(A)��ȡ(B)��Һ(C)����(D)���ȷֽ�(E)����(F)����
���и�������ķ�����ᴿӦѡ���������ַ�������ʣ� ����ѡ�÷����ı�����������ڣ�
(1)��ȥCa(OH)2��Һ��������CaCO3��( )
(2)�ѱ���ʳ��ˮ�е�ʳ����ȡ����( )
(3)��ȥ�ƾ����ܽ����ʳ��( )
(4)�ѵ�ˮ�еĵ���ȡ����( )
(5)������ˮ��ȡҽ������ˮ( )
(6)��ȥ�������е�̼���( )
(7)������ͺ�ˮ�Ļ����( )
�ο��𰸣�(1)C
(2)E
(3)F
(4)A
(5)F
(6)D
(7)B
���������
�����Ѷȣ�һ��
2������� �� 12�֣���ȥ�±�����Һ�к��е��������ʣ������ڣ���д�±���
���ʣ����ʣ�
| �����������Լ�
| ���ӷ���ʽ
|
Fe2O3��Al2O3��
| ?
| ?
|
FeCl2��Һ��FeCl3��
| ?
| ?
|
NaHCO3��Һ(Na2CO3��
| ?
| ?
�ο��𰸣����Լ���2�֣�����ʽ��2�֣���12�֣�
���ʣ����ʣ�
���������Լ�
���ӷ���ʽ
Fe2O3��Al2O3��
NaOH��Һ
Al2O3+2OH?=2AlO2?+H2O
FeCl2��Һ��FeCl3��
����
Fe+2Fe3+=3Fe2+
NaHCO3��Һ��Na2CO3��
CO2����
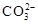 +CO2+H2O=2 +CO2+H2O=2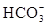
�����������
�����Ѷȣ�һ��
3��ѡ���� ����ʵ�鷽���������ǣ�������
A���ñ���̼������Һ��ȥ������̼�е������Ȼ���
B�����Ҵ���Ũ�����ȥ���������е���������
C��Ϊ�˼���������ϩ��������ֱ�ͨ��ʢ������������Ȼ�̼��Һ
D���÷�Һ©�����뱽�����Ȼ�̼�Ļ����Һ
�ο��𰸣�A��������̼�뱥��̼���Ʒ�Ӧ��Ӧ���������ͨ������̼��������Һ���ӣ���A����
B���Ҵ�������ķ�ӦΪ���淴Ӧ��Ӧ�ñ���̼������Һ���ӣ���B����
C����ϩ�����巢���ӳɷ�Ӧ���ɽ��������ͨ��������Ȼ�̼��Һ���ӣ���C��ȷ��
D���������Ȼ�̼���ܣ������÷�Һ�ķ������룬Ӧ�������룬��D����
��ѡC��
���������
�����Ѷȣ�һ��
4��ѡ���� ����ʵ����˵����ȷ���ǣ�������
A�����������У�Ӧʹ������е�ˮδ��ȫ����ʱ����ֹͣ����
B��������FeCl3��Һ������е�NaOH��Һ�У��Ӷ��Ƶ�Fe��OH��3����
C�����˲��������������뽺�����Һ
D����ʼ����ʱ��Ӧ���ȼ���������ƿ���ٿ�����ˮ��������ϣ�Ӧ���ȹ�����ˮ�ٳ��ƾ���
�ο��𰸣�AC
���������
�����Ѷȣ���
5������� ��1����ȥNaHCO3��Һ�л��е�Na2CO3����Ӧ�Ļ�ѧ����ʽ______��
��2����ȥNa2CO3�����л��е�NaHCO3����Ӧ�Ļ�ѧ����ʽ______��
��3����ȥCO2�����л��е�HCl����Ӧ�����ӷ���ʽ______��
��4����ȥFe2O3�л��е�Al2O3����Ӧ�����ӷ���ʽ______��
��5����ȥFeCl3��Һ�л��е�FeCl2����Ӧ�����ӷ���ʽ______��
�ο��𰸣���1����ȥNaHCO3��Һ�к��е�Na2CO3���ʿ�����Һ��ͨ�����������̼���壬Na2CO3��Һ���������̼��Ӧ����NaHCO3����ѧ����ʽ��Na2CO3+H2O+CO2�T2NaHCO3���ʴ�Ϊ��Na2CO3+H2O+CO2�T2NaHCO3��
��2��NaHCO3���ȶ��������ֽ⣬���ü��ȵķ������ӣ���Ӧ�ķ���ʽΪ2NaHCO3��.Na2CO3+H2O+CO2�����ʴ�Ϊ��2NaHCO3��.Na2CO3+H2O+CO2����
��3����������̼�����Ʋ�������Ӧ����̼�������ܹ����Ȼ��ⷢ����Ӧ����Ӧ�����ӷ���ʽΪ��H++HCO3-=CO2��+H2O���ʴ�Ϊ��HCO3-+H+�TH2O+CO2����
��4��������Ϊ�������������ǿ�Ӧ����Ӧ�����ӷ���ʽΪAl2O3+2OH-=2AlO2-+H2O���ʴ�Ϊ��Al2O3+2OH-�T2AlO2-+H2O��
��5����ȥFeCl3�л��е�FeCl2���ɼ����������������������µ���������ѡ����������Ӧ�����ӷ���ʽΪCl2+2Fe2+=2Fe3++2Cl-���ʴ�Ϊ��2Fe2++Cl2�T2Fe3++2Cl-��
���������
�����Ѷȣ�һ��
|