1������� ��10�֣���ҵ���Ի�����Ϊԭ������������Ҫ��Ϊ�����ν��У������ա������������ա���ش����и����⣺
��1�����ջ������γɵ�¯�����뾭������ϴ�ӡ���������?�����豸���ƣ�
��2���������η�Ӧ2SO2(g)+O2(g)  2SO3(g)����H��0��550 ��ʱ��SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��
2SO3(g)����H��0��550 ��ʱ��SO2ת��ΪSO3��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��
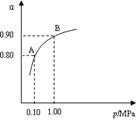
������Ҫ���SO2��ת���ʣ���Ӧ������Ӧ��?�� ����ѹ����ߡ������͡������� ������ͨ������¹�ҵ�����в��ó�ѹ��ԭ����?��
��2.0 mol SO2��1.0 mol O2����5 ���ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10 M Pa���÷�Ӧ��ƽ�ⳣ������?��
��3��Ϊѭ�����ô�����������Ա����������һ�����ӽ��������շ����¹��գ������ʴ�91.7%���ϡ���֪�Ϸ������к���V2O5��VOSO4�������Բ�������������֪��VOSO4������ˮ��V2O5������ˮ��NH4VO3������ˮ���ù��յ���������ͼ��
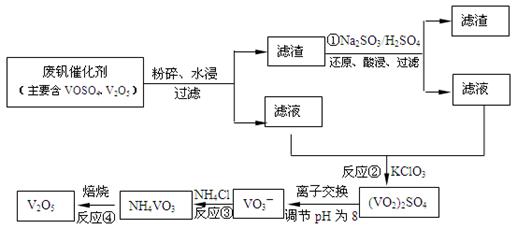
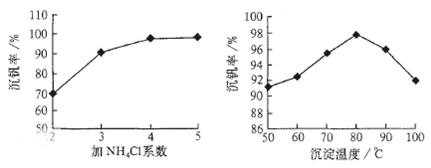
��Ӧ�٢ڢۢ�������������ԭ��Ӧ����?����������ţ�����Ӧ�۵����ӷ���ʽΪ?���ù����з�Ӧ�۵ij����ʣ��ֳƳ����ʣ��ǻ��շ��Ĺؼ�֮һ�������ʵĸߵͳ�����ҺpHӰ���⣬����Ҫ�����Ȼ��ϵ��(NH4Cl������������Һ��V2O5��������)���¶ȡ�������ͼ�Խ�������Ȼ��ϵ�����¶ȣ�?��?��
�ο��𰸣���1���Ӵ���?��2����?ʹ�ó�ѹSO2�Ϳ��Դﵽ�ϸߵ�ת���ʡ�?��3�� 400mol2/L2 .?
��4���٢�?NH4+ + VO3-==NH4VO3�� ?4��80�档
�����������1�����ջ������γɵ�¯�����ڽӴ����н��д�����ʵ��ġ���SO2�����Ĺ�����������Щ������������Ҳ����������ж������Ա��뾭������ϴ�ӡ���������Ӵ��ҡ���2�����ڷ�Ӧ2SO2(g) +O2(g)  2SO3(g)����H��0������ӦΪ���ȷ�Ӧ������Ϊ�����ԭ�ϵ������ʣ���ӦӦ���ڵ����½��С��÷�Ӧ������ӦΪ���������С�ķ�Ӧ������ѹǿ��ʹƽ�������ƶ�����Ӧ���ת������ߣ�������������ѹǿ���豸��Ҫ����ѹǿ��Ҫ����ߣ���Ҫ�Ķ���Ҳ���������Ҫ����Ͷ�룬������ȡ�������������������˵�������㡣������ʹ�ó�ѹSO2�Ϳ��Դﵽ�ϸߵ�ת���ʡ��ڷ�Ӧ��ʼʱc (SO2)=0.4mol/L;c(O2)=0.2mol/L�����ڷ�Ӧ��ƽ�����ϵ��ѹǿΪ0.10 M Pa����ʱSO2��ƽ��ת����Ϊ0.8.��ƽ��ʱc (SO2)=0.08mol/L��c(O2)=0.04mol/L��c (SO3)=0.32mol/L����˸÷�Ӧ�Ļ�ѧƽ�ⳣ��K=
2SO3(g)����H��0������ӦΪ���ȷ�Ӧ������Ϊ�����ԭ�ϵ������ʣ���ӦӦ���ڵ����½��С��÷�Ӧ������ӦΪ���������С�ķ�Ӧ������ѹǿ��ʹƽ�������ƶ�����Ӧ���ת������ߣ�������������ѹǿ���豸��Ҫ����ѹǿ��Ҫ����ߣ���Ҫ�Ķ���Ҳ���������Ҫ����Ͷ�룬������ȡ�������������������˵�������㡣������ʹ�ó�ѹSO2�Ϳ��Դﵽ�ϸߵ�ת���ʡ��ڷ�Ӧ��ʼʱc (SO2)=0.4mol/L;c(O2)=0.2mol/L�����ڷ�Ӧ��ƽ�����ϵ��ѹǿΪ0.10 M Pa����ʱSO2��ƽ��ת����Ϊ0.8.��ƽ��ʱc (SO2)=0.08mol/L��c(O2)=0.04mol/L��c (SO3)=0.32mol/L����˸÷�Ӧ�Ļ�ѧƽ�ⳣ��K=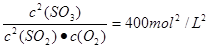 (3)�ڷϷ���������Ҫ��VOSO4��V2O5���������顢ˮ�������˵õ��������к���V2O5�������м���Na2SO3��H2SO4������������ԭ��Ӧ��V2O5��Ϊ������ˮ��VOSO4��������Һ�С�����Һ�м���KClO3,����������Ӧ��Ӧ���õ�(VO2)2SO4����(VO2)2SO4��VO3����NH4VO3��V2O5��V�Ļ��ϼ۶���+5�ۣ����ϼ۲��䣬�����Ƿ�������ԭ��Ӧ����˷�Ӧ�٢ڢۢ�������������ԭ��Ӧ���Ǣ٢�?���з�Ӧ�۵����ӷ���ʽΪNH4+ + VO3-=NH4VO3�� ��������Ŀ�ṩ��ͼ���֪�������Ȼ��ϵ����4���¶�Ϊ80�� ����ʱ��������ߡ�
(3)�ڷϷ���������Ҫ��VOSO4��V2O5���������顢ˮ�������˵õ��������к���V2O5�������м���Na2SO3��H2SO4������������ԭ��Ӧ��V2O5��Ϊ������ˮ��VOSO4��������Һ�С�����Һ�м���KClO3,����������Ӧ��Ӧ���õ�(VO2)2SO4����(VO2)2SO4��VO3����NH4VO3��V2O5��V�Ļ��ϼ۶���+5�ۣ����ϼ۲��䣬�����Ƿ�������ԭ��Ӧ����˷�Ӧ�٢ڢۢ�������������ԭ��Ӧ���Ǣ٢�?���з�Ӧ�۵����ӷ���ʽΪNH4+ + VO3-=NH4VO3�� ��������Ŀ�ṩ��ͼ���֪�������Ȼ��ϵ����4���¶�Ϊ80�� ����ʱ��������ߡ�
�����Ѷȣ�һ��
2��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�������
A��ͭ����������Һ��Ӧ��Cu+Ag+=Cu2++Ag
B������������������Һ��Ӧ��H++SO42-+Ba2++OH-=BaSO4��+H2O
C��̼��������ᷴӦ��CO32-+2H+=CO2��+H2O
D������ʯ��ˮ�м���̼������Һ��Ca2++CO32-�TCaCO3��
�ο��𰸣�A��ͭ����������Һ��Ӧ���ӷ���ʽΪ��Cu+2Ag+=Cu2++2Ag����A����
B������������������Һ��Ӧ���ӷ���ʽΪ��2H++SO42-+Ba2++2OH-=BaSO4��+2H2O����B����
C��̼��������ᷴӦ���ӷ���ʽ��CaCO3+2H+=CO2��+H2O+Ca2+����C����
D������ʯ��ˮ�м���̼������Һ��Ӧ����̼��ƺ��������ƣ���Ӧ���ӷ���ʽΪ��Ca2++CO32-�TCaCO3������D��ȷ��
��ѡD��
���������
�����Ѷȣ���
3��ѡ���� ���ӷ���ʽBa2++SO42-��BaSO4����ʾ���ǣ�?��
A�������������������������Һ֮��ķ�Ӧ
B����������������ķ�Ӧ
C�������Ա��κͿ�������������Һ֮��ķ�Ӧ
D������ͱ���ֻ����BaSO4�����ķ�Ӧ
�ο��𰸣�C
���������Ba2+�����ڿ����Եı�����Һ��SO42-�����ڿ�������������Һ��
�����Ѷȣ���
4��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A������ͨ��ˮ�У�Cl2 + H2O  2H+ + Cl��+ClO��
2H+ + Cl��+ClO��
B���������������м���HI��Һ��Fe(OH)3 + 3H+ = Fe3+ + 3H2O
C��NaAlO2��Һ��ͨ�����CO2��2AlO2��+ CO2 + 3H2O = 2Al(OH)3��+ CO32��
D����ϡ�����ȥ�Թ��ڱ�����3Ag+ 4H+ + NO3�� = 3Ag+ + NO�� +2H2O
�ο��𰸣�D
���������A��������Ϊ���ᣬд��ѧʽ������B�������Ӱ�Fe3+��ԭΪ�������ӣ�����C��������CO2Ӧ����HCO3��������D����ȷ��
�����Ѷȣ�һ��
5������� ��������ɸ�������ɺ����ʽ��з��ࣺ
��������
�μ����������⻯�
��1��������ʾ�����ʷ����������?��
��2����Na��K��H��O��S��N�������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ������±��Тڢۢ��森��������дһ����ѧʽ���ɣ�
| ������� | �� | �� | �� | ������ | �⻯��
��ѧʽ
��HCl
��?
��?
��Ba��OH��2
��Na2CO3
��?
��CO2
��Na2O
��NH3
��H2O
|
��3��д����ת��Ϊ�ݵĻ�ѧ����ʽ��?��
��4��д������۷�Ӧ�����ӷ���ʽ��?��
��5��д������෴Ӧ�����ӷ���ʽ��?��
�ο��𰸣�
���������
�����Ѷȣ�һ��