1、填空题 某综合实验小组来自来水厂参观,了解到源水处理成自来水的工艺流程示意图如
下图所示:

提供的试剂:饱和K2CO3溶液、NaOH溶液、Ba(NO3)2溶液、75%的乙醇、生石灰、CCl4、BaCl2溶液
(1)为除去源水中含有Ca2+、Mg2+、HCO3-、Cl-、SO42-等离子,选出a所代表的试剂,按加入的顺序依次为?(只填化学式)。
(2)加入凝聚剂可以除去其中的悬浮固体颗粒,该过程是?(选填下列各项的序号)。
A.只有物理变化,无化学变化
B.只有化学变化,无物理变化
C.既有化学变化,又有物理变化
FeSO4・7H2O是常用的凝聚剂,加入后最终生成红褐色胶状沉淀,则这种胶状沉淀的化学式为?。
(3)通入气体CO2的目的是?和?。
(4)下列物质中,可用来代替气体Cl2的是?(填写序号)。
① ClO2?② O3?③ 浓氨水?④ SO2?⑤ 浓硫酸
参考答案:(12分,每空2 分)(1)BaCl2;CaO(2分)?(2)C?(2分)、Fe(OH)3(2分)
(3)除去Ca2+、调节溶液的pH;(4分)?(4)①?②?(2分,见错不给分)
本题解析:(1)生石灰溶于水生成氢氧化钙,氢氧化钙和镁离子结合生成氢氧化镁白色沉淀,和HCO3-反应生成CO32-,进而生成碳酸钙沉淀,而SO42-能和Ba2+结合生成白色沉淀硫酸钡。又因为过量的Ba2+需要CO32-除去,所以按加入的顺序依次为BaCl2、CaO。
(2)混凝剂能生成具有吸附性能的胶体,该过程是化学变化。水的净化过程是物理变化,所以答案选C。亚铁离子具有还原性,能被氧化生成铁离子,所以红褐色沉淀是氢氧化铁。(3)通入二氧化碳,增大溶液中碳酸根离子浓度,则与钙离子反应生成沉淀,从而除去钙离子,并降低溶液的碱性,调节溶液的酸碱度。
(4)氯气具有强氧化性,能杀菌消毒,则作为Cl2的替代品的物质需具有强氧化性,选项中只有①②④具有强氧化性,但④中浓硫酸具有腐蚀性,不能作为自来水的消毒,则只有①②符合题意,因此答案为①②。
点评:该题紧密联系生活实际,贴近生活,针对性强,属于中等难度的试题,有利于调动学生的学习兴趣和学习积极性。明确净化原理及各物质的性质、发生的化学反应是解答本题的关键。
本题难度:一般
2、选择题 除去SO2中的SO3,并得到纯净的SO2,最好使混合气体通过
A.水
B.NaHSO3饱和溶液
C.NaHCO3饱和溶液
D.98.3%浓硫酸
参考答案:D
本题解析:三氧化硫易溶于水能被浓硫酸吸收,而二氧化硫在浓硫酸中是不能溶解的,可用浓硫酸干燥,所以正确的答案选D。
本题难度:简单
3、选择题 下列装置或操作能达到实验目的(必要的夹持装置及石棉网已省略)的是

| 
| 
| 
|
A.实验室制乙烯
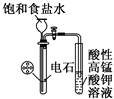
| B.实验室制乙炔
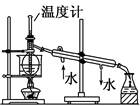
| C.实验室中分馏石油
| D.分离水和苯的混合物
并验证其还原性
|
?
参考答案:D
本题解析:制备乙烯必须用温度计插在液面以下控制温度在170℃,否则副产物较多得不到乙烯所以A错。B中电石大都不纯还含有硫化物或磷化物都可以与水反应产生的气体使高锰酸钾褪色所以B错。C中分馏石油温度计应放在支管口处测馏分的温度因此C错,D因为水和苯不互溶分层苯在上层,所以可以用分液漏斗分离,因此D正确。
本题难度:简单
4、填空题 为了达到下表所列的一些有关家庭常用物质的实验要求,请选择合适的化学试剂,将其标号填入答题卡中。
供选择的化学试剂:
A.酸性高锰酸钾
B.硝酸银溶液和硝酸
C.氢氧化钠溶液
D.无水硫酸铜粉末