1、选择题 下列事实的解释正确的是
[? ]
A.浓H2SO4和浓盐酸混合可制HCl气体,是利用了浓H2SO4的强酸性
B.SO2使溴水褪色,是利用了SO2的漂白性
C.将SO2、SO3混合气体通入氯化钡溶液中,出现浑浊,是因为有BaSO4生成
D.反应“CuSO4+H2S =CuS↓+H2SO4”能进行,是利用了较强酸制较弱酸的原理
2、选择题 下列说法中正确的是?
[? ]
A.氯气通入澄清石灰水中,制取漂粉精?
B.可用化合反应的方法制取Fe(OH)3
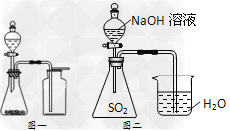
C.选择合适的试剂,用图一所示装置可分别制取少量CO2、NO和O2
D.图二装置证明SO2与NaOH发生了反应(系统装置不漏气)
3、选择题 下列性质中:
①漂白性?②氧化性和还原性?③能跟氢氧化钠溶液反应.④能使湿润的红色石蕊试剂变蓝.
二氧化硫具有的是( )
A.①④
B.③④
C.①②③
D.①②③④
4、简答题 某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
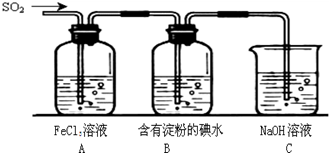
(1)SO2气体还原Fe3+生成的还原产物是?(填离子符号),参加反应的SO2和Fe3+的物质的量之比是?.
(2)下列实验方案适用于在实验室制取所需SO2的是?(双选,填序号).
A.Na2SO3溶液与HNO3?B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧?D.铜与热浓H2SO4
(3)装置C的作用是?.
(4)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有?(双选,填序号).
A.蒸发皿?B.石棉网?C.漏斗?D.烧杯?E.玻璃棒?F.坩埚
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去.
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀.
上述方案不合理的一个是?,原因是?.
(6)上述装置中能表明I-的还原性弱于SO2的现象是?.
5、选择题 气体甲通入溶液乙中时,随着甲的通入,溶液乙的颜色逐渐褪去,下列说法正确的是
[? ]
A.气体甲一定具有漂白性
B.溶液乙褪色后,不可能再恢复原来的颜色
C.气体甲可能与溶液乙中的某种有色物质发生化合反应
D.气体甲可能被溶液乙中的某些离子氧化