1、选择题 NA表示阿伏加德罗常数,下列叙述中正确的是
A.标准状况下2.24 L三氯甲烷含有分子数目为0.1 NA
B.1mol18O2、16O3混合气体中定含有40NA个质子
C.常温下,100 mL 1 mol・L―1的Na2CO3溶液中的阴离子数目大于0.1NA
D.3.2 g硫与铜充分反应,电子转移总数为0.1NA
参考答案:C
本题解析:A、标准状况下,三氯甲烷是液态,不能适用于气体摩尔体积,A不正确;B、氧气与臭氧都是氧元素形成的不同单质,由于1mol18?O2、16O3混合气体中二者的体积之比不能确定,因此不能确定质子数,B不正确;C、碳酸钠溶于水水解,方程式是CO32-+H2O HCO3-+OH-,即水解过程是阴离子增加的,所以常温下,100 mL 1 mol・L―1的Na2CO3溶液中的阴离子数目大于0.1NA,C正确;D、铜和S反应生成Cu2S,所以3.2 g硫与铜充分反应,转移电子的物质的量是
HCO3-+OH-,即水解过程是阴离子增加的,所以常温下,100 mL 1 mol・L―1的Na2CO3溶液中的阴离子数目大于0.1NA,C正确;D、铜和S反应生成Cu2S,所以3.2 g硫与铜充分反应,转移电子的物质的量是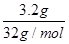 ×2=0.2mol,因此个数为0.2NA,D不正确,答案选C。
×2=0.2mol,因此个数为0.2NA,D不正确,答案选C。
本题难度:一般
2、选择题 某学生配制一定物质的量浓度的氢氧化钠溶液后,经测定发现溶液浓度偏低。该学生找出以下原因,其中不会使溶液浓度偏低的是:
[?]
A、没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中
B、容量瓶刚用蒸馏水洗净,没有烘干
C、定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切。
D、把配好的溶液倒入刚用蒸馏水洗净的试剂瓶中备用
参考答案:B
本题解析:
本题难度:简单
3、选择题 设 NA为阿伏加德罗常数的数值,下列说法正确的是(?)
A.NA个CH4分子的质量为16g/mol
B.1mol/LNaCl溶液含有NA个Na+
C.等物质的量的N2和CO所含分子数、原子个数、电子总数均相同
D.22.4LCO2中含有 NA个CO2分子
参考答案:C
本题解析:质量单位是g,A错误;1mol/LNaCl溶液中c(Na+)=1mol/L,B错误;CO和N2是等电子体,物质的量相同的CO和N2分子数、原子数、电子数均相同,C正确;D项少标准状况,D错误。
点评:原子数相同、价电子数相同的微粒互为等电子体;标准状况下,1mol任何气体的体积约是22.4L。
本题难度:一般
4、选择题 下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是(?)
A.100mL 0.5mol/L MgCl2溶液
B.200mL 0.25mol/L AlCl3溶液
C.50ml 1mol/L NaCl溶液
D.25ml 0.5mol/L HCl溶液
参考答案:D
本题解析:溶液的浓度与溶液的体积无关,0.5mol/L NaCl溶液所含的Cl-物质的量浓度为0.5mol/L;0.5mol/L MgCl2溶液Cl-物质的量浓度1mol/L;0.25mol/L AlCl3溶液Cl-物质的量浓度0.75mol/L;1mol/L NaCl溶液Cl-物质的量浓度1mol/L;0.5mol/L HCl溶液Cl-物质的量浓度0.5mol/L;
本题难度:一般
5、选择题 (1)相同质量的SO2、SO3的物质的量之比为____________;氧原子的个数之比为_ _______。
(2)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量是________;A的相对原子质量是____________;ACl2的化学式是__________。
参考答案:(1)5∶4 5∶6 (2)95 g・mol-1 24 MgCl2
本题解析:(1)根据 n=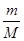 可知,相同质量的SO2、SO3的物质的量之比=
可知,相同质量的SO2、SO3的物质的量之比=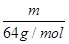 :
: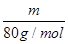 =5∶4;氧原子的个数之比=5×2∶4×3=5∶6。
=5∶4;氧原子的个数之比=5×2∶4×3=5∶6。
(2)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的物质的量=0.4mol÷2=0.2mol,因此根据n=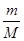 可知,该化合物的摩尔质量M=19.2g÷0.2mol=95 g/mol;氯元素的相对原子质量35.5,所以A的相对原子质量=95-35.5×2=24,因此A是Mg,则该化合物的化学式是MgCl2。
可知,该化合物的摩尔质量M=19.2g÷0.2mol=95 g/mol;氯元素的相对原子质量35.5,所以A的相对原子质量=95-35.5×2=24,因此A是Mg,则该化合物的化学式是MgCl2。
考点:考查物质的量的有关计算、化学式确定
本题难度:一般