|
高中化学必备知识点《物质的量》高频试题特训(2020年最新版)(八)
2021-06-11 06:28:58
【 大 中 小】
|
1、选择题 下列叙述中正确的是
①标准状况下,1 L HCl和1 L H2O的物质的量相同
②标准状况下,1 g H2和14 g N2的体积相同
③28 g CO的体积为22.4 L
④两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑤在同温同体积时,气体物质的物质的量越大,则压强越大
⑥同温同压下,气体的密度与气体的相对分子质量成正比
A.①②③
B.②⑤⑥
C.②③⑥
D.④⑤⑥
|
参考答案:B
本题解析:①标准状况下,水不是气体,所以1 L HCl和1 L H2O的物质的量不相同,错误;②标准状况下,1 g H2的物质的量是0.5mol,14 g N2的物质的量也是0.5mol,根据阿伏伽德罗定律,相同条件下,物质的量相同的任何气体的体积相同,正确;③28 g CO的物质的量是1mol,但未指明标准状况,所以体积不一定为22.4 L,错误;④两种物质的物质的量相同,则它们在标准状况下的体积不一定相同,当二者都是气体时,体积相同,错误;⑤在同温同体积时,气体物质的物质的量越大,则压强越大,正确;⑥同温同压下,气体的摩尔体积相同,所以气体的密度与气体的相对分子质量成正比,正确,答案选B。
考点:考查对阿伏伽德罗定律的理解应用
本题难度:一般
2、简答题 将3.22g芒硝(Na2SO4?10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为多少克?
参考答案:3.22g芒硝的物质的量为3.22g322g/mol=0.01mol
所以溶液中n(Na+)=2n(Na2SO4?10H2O)=0.01mol×2=0.02mol
每100个水分子中溶有1个钠离子,所以n(H2O)=100n(Na+)=2mol
0.01molNa2SO4?10H2O中含有水的物质的量为0.01mol×10=0.1mol
所以需要的水的物质的量为2mol-0.1mol=1.9mol
所以需要水的质量为1.9mol×18g/mol=34.2g
答:需要水的质量为34.2g.
本题解析:
本题难度:一般
3、选择题 配制一定物质的量浓度的NaCl溶液时,造成浓度偏低的原因可能是( )
A.定容摇匀后,有少量溶液外流
B.定容时,俯视液面
C.称量时,在天平托盘上放上称量纸,将NaCl固体放在纸上称量
D.溶解NaCl的烧杯未洗涤
参考答案:A、定容摇匀后,有少量溶液外流,由于已经摇匀,即便有少量的液体流出,不会影响配制溶液的浓度,故A错误;
B、定容使俯视液面,会导致加入的蒸馏水体积偏小,根据c=nV可得,配制的溶液浓度偏高,故B错误;
C、称量时,在天平托盘上放上称量纸,将NaCl固体放在纸上称量,该操作合理,不会对配制结果产生影响,故C错误;
D、溶解NaCl的烧杯未洗涤,导致配制的溶液中溶质的物质的量偏小,根据c=nV可得,配制溶液浓度浓度偏低,故D正确;
故选D.
本题解析:
本题难度:一般
4、选择题 下列有关说法正确的是(?)
A.9.2 g NO2气体中含有分子数目为0.2NA
B.标准状况下,2.24 L SO3中含有氧原子数目为0.3NA
C.2 g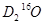 中含中子、质子、电子数目均为NA 中含中子、质子、电子数目均为NA
D.标准状况下2.24 L Cl2通入足量水中或NaOH溶液中,转移电子数目均为0.1NA
参考答案:C
本题解析:A项,存在2NO2 N2O4,9.2 g NO2气体中含有的分子数目应小于0.2NA;B项,标况下,SO3为固体;C项, N2O4,9.2 g NO2气体中含有的分子数目应小于0.2NA;B项,标况下,SO3为固体;C项,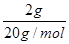 =0.1 mol,中子数为NA,质子数为NA,电子数为NA,正确;D项,Cl2和H2O的反应为可逆反应。 =0.1 mol,中子数为NA,质子数为NA,电子数为NA,正确;D项,Cl2和H2O的反应为可逆反应。
本题难度:一般
5、选择题 用NA表示阿伏伽德罗常数的数值,下列说法正确的是
A.标准状况下,11.2LH2O所含的水分子数目为0.5NA
B.16gO2和O3的混合气体中所含的氧原子数目为NA
C.1.00mol/LNa2CO3溶液中所含Na+的数目为2NA
D.0.1molZn与含0.1molHCl的盐酸充分反应,产生H2数目为0.2NA
参考答案:B
本题解析:略
本题难度:一般
|