1������� �������ֶ�����Ԫ��X��Y��Z��W�����У�
�� X��Wԭ�ӵĵ��Ӳ���������������֮�ȷֱ�Ϊ3:1��1:3
�� Yԭ����Ԫ�����ڱ���ԭ�Ӱ뾶��С��
�� Z���γɻ�������������Ԫ��
�ش��������⣺
��1��XԪ�������ڱ��е�λ���������������������� ����
��2����������Ԫ����������ɵĺ��зǼ��Թ��ۼ��Ļ�����ķ���ʽ��������������������һ�ּ��ɣ���
��3��������X2W2�ĵ���ʽ�������������� ��
��4����1 mol Na2SiO3����Һ�л���ͨ��2 mol��ZO2����Ӧ�����ӷ���ʽ������������ ����
��5����Y��Z��WԪ���е����ֻ����ֿ�����ɶ��ַ��ӣ����к���10�����ӵķ�����_________���ѧʽ����
��6����25.00 mL��Y2Z2W4��Һ�м���5.00 mL 0.50 mol/L����KMnO4��Һǡ����ȫ��Ӧ���õ�ZO2��Mn2+�������Y2Z2W4��Һ�����ʵ���Ũ������������ ��mol/L��
�ο��𰸣���12��ÿ�ն��֣���1���������ڡ��ڢ�A��?��2��H2O2��C2H6
��3��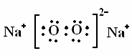 ?��4��2CO2 + 2 H2O + SiO32����2 HCO3��+ H2SiO3��
?��4��2CO2 + 2 H2O + SiO32����2 HCO3��+ H2SiO3��
��5��H2O��CH4��6��0.25
���������Yԭ����Ԫ�����ڱ���ԭ�Ӱ뾶��С�ģ���Y����Ԫ�ء�Z���γɻ�������������Ԫ�أ����Z��̼Ԫ�ء�X��Wԭ�ӵĵ��Ӳ���������������֮�ȷֱ�Ϊ3:1��1:3�����ھ��Ƕ�����Ԫ�أ���˵��X�ǵ�������Ԫ�أ�����Ԫ�ء�W�ǵڶ�����Ԫ�أ�����Ԫ�ء�
��1��NaԪ�ص�ԭ��������11�������ڱ��е�λ���ǵ������ڡ��ڢ�A�塣
��2����������Ԫ����������ɵĺ��зǼ��Թ��ۼ��Ļ�����ķ���ʽH2O2��C2H6��
��3��������X2W2�ǹ������ƣ��������Ӽ��ͷǼ��Լ������ӻ��������ʽ��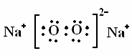 ��
��
��4��̼�������ǿ�ڹ���ģ�����1 mol Na2SiO3����Һ�л���ͨ��2 mol��CO2����Ӧ�����ӷ���ʽ��2CO2 + 2 H2O + SiO32����2 HCO3��+ H2SiO3����
��5����Y��Z��WԪ���е����ֻ����ֿ�����ɶ��ַ��ӣ����к���10�����ӵķ�����H2O��CH4��
��6���ڷ�Ӧ��̼Ԫ�صĻ��ϼ۴ӣ�3�����ߵ���4�ۣ�ʧȥ1�����ӡ���Ԫ�صĻ��ϼ۴ӣ�7�۽��͵���2�ۣ��õ�5�����ӣ����Ը��ݵ��ӵĵ�ʧ�غ��֪��0.025L��c��2��0.005L��0.50mol/L��5�����c��0.25mol/L��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ�������������ѧ����������������Ӧ�������������ԡ����ڱ���Ԫ�ص��ƶϡ�Ϊ���壬����ѧ����Ԫ�����ڱ�����Ϥ�̶ȼ���Ա��и�Ԫ�����ʺ���Ӧԭ�ӽṹ�������Եݱ���ɵ���ʶ�����ճ̶ȡ�������ѧ�������ʽṹ�����ʹ�ϵ�Լ�����Ԫ�������ɽ�����廯ѧ���������
�����Ѷȣ�һ��
2��ѡ���� (˫ѡ)ijԪ��X��ԭ������Ϊ52,����������ȷ����(����)��
A��X����Ҫ���ϼ���-2��+4��+6
B��X�����γ��ȶ�����̬�⻯��
C��X������������Ӧˮ��������Ա�HBrO4������ǿ
D��X�ļ������ӵĻ�ԭ�Ա�������ǿ
�ο��𰸣�AD
�������������Ԫ�����ڱ���֪52��Ԫ��λ�ڵ������ڵڢ�A��,λ�ڷǽ����ͽ������紦�Ϸ�,Ϊ�ǽ���Ԫ��,�ǽ����Խ���,�仯�ϼ���������Ϥ��S����,A��;��̬�⻯����ȶ��Խϲ�,B��;XԪ����Br�����·�,�ǽ����Ա�Br��,����������Ӧˮ��������Ա�HBrO4��;X�������Ա�����,�������ӵĻ�ԭ�Ա�Br-ǿ��
�����Ѷȣ���
3������� ��16�֣�A��B��C��D���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶D��C��A��B,����A��B����ͬһ���ڣ�A��C����ͬһ���塣Cԭ�Ӻ��ڵ�����������A��Bԭ�Ӻ��ڵ�������֮�ͣ�Cԭ��������������Dԭ��������������4�����Իش��������⣺
��1��������Ԫ�طֱ��ǣ�A?��B?��C?��D?��
��2��������Ԫ�������γɵ���̬�⻯����ȶ����ɴ�С��˳����?
?��������̬�⻯��Ļ�ѧʽ��ʾ��
��3��A��B�γɵ���ԭ�ӷ��ӵĻ�ѧʽ��?��B��D�γɵļ������Ӽ��ֺ��й��ۼ��Ļ�����Ļ�ѧʽ��?��
��4��AԪ�ص�ij��������DԪ�ص�ij���������ﷴӦ���ɵ��ʵĻ�ѧ����ʽ��?
?��
�ο��𰸣�(1)̼?��?��?��?
(2)H2O��CH4��SiH4?
(3)CO2? Na2O2
(4)2CO2+2Na2O2====2Na2CO3+O2��
�����������
�����Ѷȣ���
4��ѡ���� ���и�����������ͬ�������͵���������?��?��
A��H3O+��NH4+��Na+��HF
B��OH-��F-��O2-��Ne
C��CH4��NH3��H2O��HF
D��O2-��F-��Mg2+��Al3+
�ο��𰸣�C
�����������
�����Ѷȣ���
5��ѡ���� ��NH4+�������������͵���������ͬ�������ǣ�?��
A��H3O+
B��NH2-
C��OH-
D��Mg2+
�ο��𰸣�A
���������NH4+�������������͵������ֱ���11��10����ѧϰABCD���������������͵������ֱ���11��10��9��10��9��10��12��10������NH4+�������������͵���������ͬ��������ѡ��A����ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣����Ĺؼ�����ȷ�������ͺ���������ļ������ݣ�����������ѧ������˼ά���������Ӧ��������
�����Ѷȣ�һ��