1、选择题 下列有关化学原理表达正确的是
A.分散系中分散质粒子的大小:Fe(OH)3悬浊液<Fe(OH)3胶体<FeCl3溶液
B.反应2CO(g)=2C(s) + O2(g)的△H>O、△S<0,可利用该反应来消除CO污染
C.室温下pH=3的盐酸与pH=11的MOH溶液等体积混合后溶液呈碱性,说明MOH为弱碱
D.NH4NO3溶液和HNO3溶液中滴加石蕊都变红色,是因为它们均能电离出H+
2、选择题 下列关于离子共存的说法不正确的是?
A.在溶液中K+、Fe3+、Cl-、S2-是因发生氧化还原反应而不能大量共存
B.在c(H+)=10-13mol/L的溶液中K+、Cl-、AlO2-、CO32-能大量共存,且加入NaHSO4溶液过程中会产生气体和沉淀
C.某透明溶液中可以存在Cu2+、NO3-、H+、SO42-
D.某溶液中加入金属铝有H2放出,则溶液中一定能大量共存K+、Mg2+、NO3-、SO42-
3、选择题 下列指定溶液中,各组离子可能大量共存的是( )
A.pH=1的溶液中:K+、Fe2+、C1-、NO3-
B.加入Al能放出H2的溶液中:NH4+、SO42-、C1-、HCO3-
C.在含有大量Fe3+的溶液中:NH4+、C1-、Na+、SCN-
D.由水电离的c(OH-)=10-13mol?L-1的溶液中:Ba2+、Na+、C1-、Br-
4、选择题 在强酸溶液中,下列各组离子能够大量共存的是
[? ]
A.Mg2+、Ca2+、HCO3-、Cl-
B.Na+、AlO2-、Cl-、SO42-
C.Cu2+、Fe3+、SO42-、MnO4-
D.K+、Fe2+、SO42-、NO3-
5、填空题 I.如图1为向25mL 0.1mol・L―1NaOH溶液中逐滴滴加0.2mol・L-1CH3COOH溶液过程中溶液pH的变化曲线。请回答:
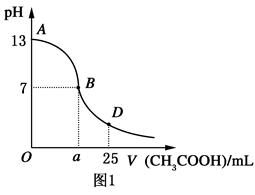
⑴ B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?________(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?________区间(若正确,此问不答)。
⑵关于该滴定实验,从下列选项中选出最恰当的一项________(选填字母)。

?
| 锥形瓶中溶液
| 滴定管中溶液
| 选用指示剂
| 选用滴定管
|
A
| 碱
| 酸
| 酚酞
| (乙)
|
B
| 酸
| 碱
| 甲基橙
| (甲)
|
C
| 碱
| 酸
| 石蕊
| (甲)
|
D
| 酸
| 碱
| 酚酞
| (乙)
|
⑶ AB区间,c(OH―)>c(H+),则c(OH―)与c(CH3COO―)大小关系是________。
A.c(OH―)大于c(CH3COO―)? B.c(OH―)小于c(CH3COO―)
C.c(OH―)等于c(CH3COO―)? D.上述三种情况都可以
⑷在D点时,溶液中c(CH3COO―)+c(CH3COOH)________2c(Na+)(填“>”“<”或“=”)。
Ⅱ.t℃时,某稀硫酸溶液中c(H+) = 10―a mol・L―1,c(OH-) = 10―b mol・L―1,已知a+b=13:
⑸该温度下水的离子积常数Kw的数值为________。
⑹该温度下(t℃),将100mL 0.1mol・L―1的稀H2SO4与100mL 0.4mol・L―1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH=________。