1、选择题 下列叙述正确的是
A.电解精炼金属时,含杂质的粗金属做阳极,与电源正极相连
B.电解池中金属导线中电子由电源的负极流向电解池的阳极,从电解池的阴极流向电源的正极
C.在电解池中,电解质溶液中的阴离子向阴极移动,阳离子向阳极移动
D.在电解精炼金属过程中,电解质溶液的成分不发生任何变化
参考答案:A
本题解析:电解池中金属导线中电子由电解池的阳极流向电源的正极,从电源的负极流向电解池的阴极,B不正确。电解池正阴离子向阳极移动,阳离子向阴极移动,C不正确。精炼金属时,金属的杂质也可能失去电子加入溶液,D不正确。答案选A。
本题难度:简单
2、选择题 按下图的装置进行电解,A极是铜锌含金,B极为纯铜。电解质溶液中含有足量的Cu2+。 通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A极合金中Cu、Zn的原子个数比为
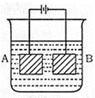
A.4:1
B.3:1
C.2:1
D.5:3
参考答案:B
本题解析:B是阴极,始终是铜离子放电析出铜。A是阳极,先是锌失去电子进入溶液,然后是铜失去电子,进入溶液。所以根据反应式Zn+Cu2++=Zn2++Cu可知每消耗1mol锌,溶液质量增加1g,所以合金中锌的物质的量是0.03mol,同时析出的铜也是0.03mol,质量是1.92g。所以合金中铜的质量是7.68g-1.92g=5.76g,物质的量是0.09mol,所以合金中Cu、Zn的原子个数比为3:1。答案选B。
本题难度:一般
3、简答题 【选修2化学与技术】(15分)
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:
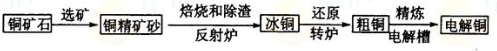
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000℃左右,黄铜矿与空气反应
生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物。该过程中两个主
要反应的化学方程式分别是 、
,反射炉内生成炉渣的主要成分是 ;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%--50%。转炉中,将冰铜加
熔剂(石英砂)在1200℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化为Cu2O,生成Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是 、 ;
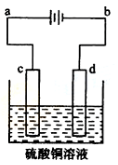
(3)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板应是图中电极_ _(填图中的字母);在电极d上发生的电极反应式为 ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为 。
参考答案:

本题解析: (1)根据题目信息可知,发生的两个主要反应分别是:2CuFeS2+O2高温Cu2S+2FeS+SO2;2FeS+3O2高温2FeO+2SO2。炉渣的主要成分有Cu2S、FeS、FeO三种物质。(2)根据题目信息可写出所发生的化学方程式分别为:2Cu2S+3O2高温2Cu2O+2SO2;2Cu2O+Cu2S高温6Cu+SO2。(3)在粗铜的精炼中,粗铜与电源正极相连作阳极,金属失去电子,变成阳离子进入溶液;精铜与电源负极相连,做负极。电极d上发生的电极反应式为:Cu2++2e- Cu。Au、Ag以单质形式存在电极C附近,Fe以Fe2+ 形式存在d电极附近。[来^源@:&%中~教网]
Cu。Au、Ag以单质形式存在电极C附近,Fe以Fe2+ 形式存在d电极附近。[来^源@:&%中~教网]
【考点定位】 电化学,电极方程式的书写,化学方程式的书写
本题难度:一般
4、填空题 电解原理在化学工业中有广泛的应用。如图表示一个电解池,?装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
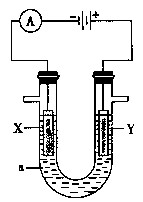
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为?,在X极附近观察到的现象是?。电解液中向X极方向移动的离子是??。
②Y电极上的电极反应式为?,
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是 ?
②Y电极的电极反应式为?(说明:杂质发生的反应不必写出。)
③溶液中的c(Cu2+)与电解前相比 ??(填“变大”、“变小”或“不变”)。
参考答案:(1)①2H2O + 2e- = H2 + 2OH-?(2H++2e-=H2↑)有气泡产生,溶液变红? Na+,H+
②2Cl- - 2e-=Cl2
(2)①精铜?②Cu-2e-=Cu2+?③变小
本题解析:(1)X电极和电源的负极相连,所以作阴极。溶液中的氢离子放电,电极反应式是2H++2e-=H2↑。氢离子放电,破坏了阴极周围水的电离平衡,导致阴极周围溶液显碱性,所以溶液显红色。电解液中向X极(阴极)方向移动的离子是阳离子:Na+,H+②Y电极和电源的正极相连,作阳极。溶液正的氯离子放电生成氯气,电极反应式是2Cl-―2e-=Cl2↑。
(2)粗铜精炼时,粗铜和电源的正极相连,作阳极。纯铜和电源的负极相连,作阴极,硫酸铜作电解质溶液,所以①X电极材料是纯铜,电极反应式是Cu2++2e-=Cu;②Y电极材料是粗铜,电极反应式是Cu-2e-=Cu2+。③阳极其他金属失电子的时候,溶液中的Cu2+ 得电子,所以精炼过程中,溶液中的c(Cu2+)变小。
本题难度:一般
5、选择题 镍氢电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镍镉电池。镍氢电池的总反应式是
1/2H2+NiO(OH)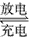 Ni(OH)2。根据此反应式判断,下列叙述正确的是
Ni(OH)2。根据此反应式判断,下列叙述正确的是
[? ]
A.电池放电时,电池负极周围溶液的碱性增强
B.电池放电时,镍元素被氧化
C.电池充电时,氢元素被还原
D.电池放电时,氢气是负极
参考答案:CD
本题解析:
本题难度:一般