1、选择题 化学试剂不变质和实验方法科学是化学实验成功的保障。下列试剂保存方法或实验方法中,不正确的是
A.实验室中金属钠通常保存在煤油里
B.氯化钠中混有少量单质碘杂质,可用升华的方法提纯
C.保存FeCl2溶液时,通常在溶液中加少量的单质铁
D.配制一定物质的量浓度的NaOH溶液时,要将NaOH固体放在滤纸上称量
参考答案:D
本题解析:钠是活泼的金属,极易和氧气和水反应,且钠的密度大于煤油的,因此实验室中金属钠通常保存在煤油里,A正确;碘单质易升华,而氯化钠熔点高,所以氯化钠中混有少量单质碘杂质,可用升华的方法提纯,B正确;氯化亚铁易被氧化生成氯化铁,所以保存FeCl2溶液时,通常在溶液中加少量的单质铁,易防止氯化亚铁被氧化,C正确;氢氧化钠易吸水,且具有腐蚀性,所以称量氢氧化钠固体时,要将NaOH固体放在烧杯上称量,D不正确,答案选D。
点评:该题是基础性实验题的考查,难度不大,有助于培养学生分析问题、解决问题的能力。该题的关键是熟练记住有关物质的性质,然后灵活运用即可。
本题难度:简单
2、实验题 (9分)实验室配制500mL0.5mol・L-1的NaOH溶液,有如下操作步骤:
①把称好的NaOH放入小烧杯中。加入适量的蒸馏水溶解、冷却;
②把①所得溶液小心转入500mL容 量瓶中;
量瓶中;
③继续向容鳍瓶中加蒸馏水 至液面距刻度线l~2cm处,改用胶头滴管小心加蒸馏水至溶液凹液面底部与刻度线相切;
至液面距刻度线l~2cm处,改用胶头滴管小心加蒸馏水至溶液凹液面底部与刻度线相切;
④用少量蒸馏水洗涤烧杯2~3次,每次洗涤的液体都小心用同一玻璃棒引流转入容最瓶并轻轻摇匀;
⑤将容 量瓶塞紧瓶塞,充分摇匀。
量瓶塞紧瓶塞,充分摇匀。
回答下列问题:
(1)要配制氢氧化钠溶液,在用托盘天平称量氢氧化钠固体时,托盘天平的读数是________
(填代号,下同);
A.10.0g?B.10.00g?C.> 10.0g?
10.0g? ? D.<10.0g
? D.<10.0g
(2)本实验操作步骤的正确顺序是(填序号)_____________________;
(3)本实验用 到的基本仪器除了天平、药匙、玻璃棒、烧杯以外,
到的基本仪器除了天平、药匙、玻璃棒、烧杯以外,
还需要的仪器有_________________;
(4)某同学观察液面的情况如图所示,对所配溶液的物质的量浓度有何影响? ____________________(填“偏高”、“偏低”或“无影响”);

(5)在配制溶液的过程中,下列操作能造成结果偏低的是________________。
A.容量瓶不干燥,含有少量蒸馏水? B.溶解所用的烧杯未洗涤
C.称量NaOH固体时,所用的砝码生锈? D.定容后摇匀,发现液面低于刻度线
参考答案:(9分)( 1)C(2分)?(2)①②③④⑤(2分)
1)C(2分)?(2)①②③④⑤(2分)
(3)500mL容量瓶、胶头滴管(各1分,共2分)
(4)偏高(1分)
(5)B(2分)
本题解析:略
本题难度:一般
3、选择题 实验室配制1mol・L-1盐酸250mL,下列不需用的仪是:
A.250ml容量瓶
B.托盘天平
C.胶头滴管
D.烧杯
参考答案:B
本题解析:盐酸是液体,不是固体,不需要称量,故不需要托盘天平,答案选B。
本题难度:简单
4、实验题 某同学用如图所示的装置进行铜与浓硫酸反应的实验。

请回答:
(1)铜与浓硫酸反应的化学方程式是________________________
(2)实验过程中,观察到品红溶液________________,石蕊溶液________________,说明SO2________(填选项)。
a. 有氧化性? b. 有还原性? c. 有漂白性? d. 水溶液显酸性
(3)为进一步确认产生的气体是二氧化硫气体,还应补充的操作是________________
(4)结合离子方程式说明试管D中氢氧化钠溶液的作用是______________________
(5)把试管A中的液体冷却后慢慢倒入盛有水的烧杯里,观察到溶液呈________色,说明铜元素被氧化生成了________离子。
参考答案:(11分)(1)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O(2分)
CuSO4+SO2↑+2H2O(2分)
(2)褪色(1分)?变红(1分)? cd(2分)?(3)加热褪色后的品红溶液(1分)
(4)吸收逸出的SO2,SO2+2OH-=SO32-+H2O(2分)
(5)蓝(1分);铜(1分,写成Cu2+给分)
本题解析:(1)浓硫酸是氧化性酸,因此铜与浓硫酸反应的化学方程式是Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
(2)还原产物SO2具有漂白性,所以SO2通入到品红溶液中,溶液红色退去;SO2溶于水生成亚硫酸,溶液显酸性,所以通入到石蕊试液中,溶液显红色。
(3)由于SO2的漂白是不稳定的,加热后又能恢复到用来到颜色,所以为进一步确认产生的气体是二氧化硫气体,还应补充的操作是加热褪色后的品红溶液。
(4)SO2有毒,属于大气污染物,所以氢氧化钠溶液的作用是吸收逸出的SO2,反应的离子方程式是SO2+2OH-=SO32-+H2O。
(5)在反应中铜是还原剂,失去电子,被氧化生成硫酸铜,所以把试管A中的液体冷却后慢慢倒入盛有水的烧杯里,观察到溶液呈蓝色。2的性质以及尾气处理等
点评:该题是高考中的常见考点,属于中等难度的试题。试题基础性强,紧扣教材,有利于巩固学生的基础,提高学生的综合实验能力,也有利于培养学生的逻辑思维能力和环境保护意识,难度不大。
本题难度:一般
5、实验题 (11分)实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题:
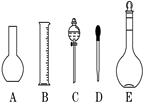
(1)如图所示的仪器中配制溶液肯定不需要的是 ?(填序号),
仪器C的名称是?,
本实验所需玻璃仪器E规格为 ?mL。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度的标准溶液
B.长期贮存溶液
C.用来加热溶解固体溶质
D.量取一定体积的液体