?
参考答案:(6分)用VSEPR理论判断:(各1分)
物质
孤对电子对数
轨道杂化形式
分子或离子的形状
NH4+
0
Sp3
正四面体
NCl3
1
Sp3
三角锥形
本题解析:由公式:孤对电子对数=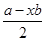 可求得NH4+为0、NCl3为1,价层电子对数分别为4、3,则轨道杂化形式均为Sp3,但微粒形状分别为正四面体和三角锥形。 可求得NH4+为0、NCl3为1,价层电子对数分别为4、3,则轨道杂化形式均为Sp3,但微粒形状分别为正四面体和三角锥形。
本题难度:一般
2、选择题 下列物质中属于离子化合物的是
A.KCl
B.Ba(OH)2
C.H2O
D.NH4Cl
参考答案:ABD
本题解析:含有离子键的化合物是离子化合物,水中只有极性键,属于共价化合物。答案是ABD。
本题难度:一般
3、选择题 下列反应中生成物总能量高于反应物总能量的是(?)
A.碳酸钙受热分解
B.乙醇燃烧
C.铝粉与氧化铁粉末反应
D.氧化钙溶于水
参考答案:A
本题解析:反应中生成物总能量高于反应物总能量的反应为吸热反应。A、碳酸钙受热分解为吸热反应,正确;B、乙醇燃烧为放热反应,错误;C、铝粉与氧化铁粉末反应放热反应,错误;D、氧化钙溶于水放热反应,错误。
本题难度:一般
4、选择题 下图是吸热反应的是( )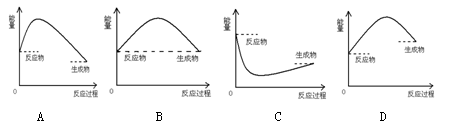
参考答案:D
本题解析:反应物的总能量低于生成物的总能量,则需要自外界吸收能量,为吸热反应。
本题难度:一般
5、选择题 能用键能知识解释的是
A.稀有气体的化学性质很不活泼
B.HCl气体比HI气体稳定
C.干冰易升华
D.HF熔沸点高于HCl
参考答案:B
本题解析:A.稀有气体是单原子分子,不存在化学键。由于原子是2电子或8电子的稳定结构,所以化学性质很不活泼。错误。B.由于非金属性Cl>I。元素的非金属性越强,其单质与氢气结合的越牢固,键能越大,相应的氢化物的稳定性就越强,因此HCl气体比HI气体稳定。正确。C.固态CO2俗称干冰。是分子晶体,依靠分子间作用力结合。升华时破坏的的是分子间作用力。由于分子间作用力比较弱,所以易升华。与化学键的键能单质无关。错误。D.HF、HCl但是分子晶体,依靠分子间作用力结合。在HF分子间除了存在分子间作用力外,还存在氢键,增加了分子之间的相互作用,使物质熔化或气化消耗的能量比HCl多。因此熔沸点高于HCl。但是这与分子内的化学键的键能大小无关。错误。
本题难度:简单
|