| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ����ɡ���ѧ��Ӧ����������Ƶ������ѵ��2020�����°棩(��)
����Լ������Ӧ  �Ħ�HΪ��384 kJ��mol-1 �Ħ�HΪ��384 kJ��mol-1�ο��𰸣�A ���������A����������1mol��������һ������������Һ̬��Ϊ��̬�����յ���������100 �桢101 kPa�����£�Һ̬ˮ��������Ϊ40.69 kJ��mol-1������������̬ת��ΪҺ̬�ͷ�����40.69 kJ����H2O(g) �����Ѷȣ�һ�� 2��ѡ���� �Ȼ�ѧ����ʽ�л�ѧʽǰ�Ļ�ѧ��������ʾ( ) |
�ο��𰸣�D
����������Ȼ�ѧ����ʽ�л�ѧʽǰ�Ļ�ѧ��������ʾ�μӷ�Ӧ�����ʵ����ʵ�������ѡD��
�����Ѷȣ�һ��
3��ѡ���� ��֪�Ȼ�ѧ����ʽ��SO2(g)+ 1/2O2(g) 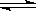 SO3(g) ��H =
SO3(g) ��H =
�ο��𰸣�
���������
�����Ѷȣ���
4��ѡ���� ���з�Ӧ������������ԭ��Ӧ����
A.Cu+4?HNO3��Ũ��Cu��NO3��2+2?NO2��+2?H2O
B.Cu+2FeCl3�TCuCl2+2FeCl2
C.��NH4��2SO4+2NaOHNa2SO4+2NH3��+2H2O
D.2FeCl3+SO2+2H2O�TH2SO4+2HCl+2FeCl2
�ο��𰸣�C
����������������е���ת�ƵĻ�ѧ��Ӧ��������ԭ��Ӧ������������Ԫ�ػ��ϼ۵��������ݴ˷������
���A���÷�Ӧ�У�ͭʧ���ӣ�����õ��ӣ������е���ת�ƣ���������ԭ��Ӧ����A��ѡ��
B���÷�Ӧ�У�ͭʧ���ӣ��Ȼ����õ��ӣ������е���ת�ƣ���������ԭ��Ӧ����B��ѡ��
C���÷�Ӧ�У���Ԫ�صĻ��ϼ۶����仯�����Բ���������ԭ��Ӧ����Cѡ��
D���÷�Ӧ�У��Ȼ����õ��ӣ���������ʧ���ӣ������е���ת�ƣ���������ԭ��Ӧ����D��ѡ��
��ѡC��
���������⿼����������ԭ��Ӧ���жϣ���ȷԪ�صĻ��ϼ��ǽⱾ��Ĺؼ����ѶȲ���
�����Ѷȣ�����
5��ѡ���� ����������ȷ���ǣ�������
A���ɱ���SiCl4�ۻ�ʱ����Ҫ�ƻ���ѧ��
B��32gS8���Ӻ�8molS-S���ۼ�
C��H2S��CS2���Ӷ��Ǻ����Լ��ļ��Է���
D��PCl3��BCl3����������ԭ�ӵ�����㶼�ﵽ8���ӽṹ
�ο��𰸣�A���ɱ���SiCl4���Ƿ��Ӿ��壬�ۻ�ʱ����Ҫ�ƻ���ѧ������A��ȷ��
B��32gS8���ӵ����ʵ���Ϊ32g256g/mol=18mol��1��S8�����к���8��S-S��������32gS8���Ӻ�1molS-S���ۼ�����B����
C��H2S����H��SԪ��֮���γɼ��Լ������ӽṹ���Գƣ�������ɵ����IJ��غϣ����ڼ��Է��ӣ�CS2����C��SԪ��֮���γɼ��Լ����ҷ��ӽṹ�Գƣ�������ɵ������غϣ����ڷǼ��Է��ӣ���C����
D��PCl3��PԪ�صĻ��ϼ���+3�ۣ�Pԭ�Ӻ�����5�����ӣ�����3+5=8��Pԭ������8���ӽṹ����ԭ�ӵĻ��ϼ���-1���仯�ϼ۵ľ���ֵ��1����1+7=8������Clԭ������8�Ľṹ��BCl3��BԪ�صĻ��ϼ���+3�ۣ�Bԭ�Ӻ�����3�����ӣ�����3+3=6��Bԭ������6���ӽṹ����ԭ�ӵĻ��ϼ���-1���仯�ϼ۵ľ���ֵ��1����1+7=8������Clԭ������8�Ľṹ����D����
��ѡ��A��
���������
�����Ѷȣ���
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ���ȫ��δ֪������.. | |
| �����Ŀ |