1������� (1)�ý�������ȡ�������ƵĻ�ѧ����ʽ�� ____��������____��
(2)��֪�ý��������������ƣ����ж��ַ�����
��4Na+ O2=2Na2O;��4Na+CO2=2Na2O+C;��2NaNO2+ 6Na=4Na2O+N2����
���������ַ�������õķ����� ____��ԭ����____��
�ο��𰸣�(1)2Na+O2 Na2O2? ��������ɫ���棬���ɵ���ɫ����
Na2O2? ��������ɫ���棬���ɵ���ɫ����
(2)�ۣ��˷�Ӧ�в���ֻ��Na2O�ǹ��壬������һ���� N2������Χ�����е������ž���ʹ��Na2O����������Na2O2
���������
�����Ѷȣ�һ��
2��ѡ���� �������ʲ����õ���ֱ�ӻ��϶��Ƶõ��ǣ�������
��Na2O2��FeCl3��NO2��Mg3N2��SO3��CO��
A���٢�
B���ڢ�
C���ۢ�
D���ܢ�
�ο��𰸣�������������Ӧ�����֣�һ������������ȼ�գ�����ȼ�����ɵ���ɫ�Ĺ������ƣ�һ�����ڳ�������������Ӧ�����ɰ�ɫ�������ƣ��ʢٴ���
��������ǿ������������ֱ�ӽ�����������Ϊ���+3�ۣ��������������Ƿ��������������Ȼ������ʢڴ���
���ڷŵ������£��������Ժ�������������һ��������N2+O2?�ŵ�?.?2NO��һ������������Ѹ�ٻ��ϣ����ɶ���������2NO+O2=2NO2���ʢ���ȷ��
���ڵ�ȼ�������£�������þ��Ӧ���ɵ���þ��Mg3N2���ʢܴ���
�����ڿ����е�ȼ���ɵ���ɫ���棬����������������ɫ���棬����SO2 ��������SO3���ʢ���ȷ��
��̼�ڿ�����ȼ�գ���ҫ�۵Ļ�ɫ���棬����CO2��ȼ�ղ���ȫ����CO���ʢ���
��ѡC��
���������
�����Ѷȣ���
3��ѡ���� �ѽ�����Ͷ�뵽�������ʵ���Һ�У���Һ����������ǣ�������
A��HCl
B��Na2SO4
C��NH4Cl
D��CuSO4
�ο��𰸣�A����Ͷ����������Һ�з�����Ӧ2Na+2H+=Na++H2�����ɷ���ʽ��֪ÿ46g�Ʒ�Ӧ����2g��������Һ��������44g����A�����ϣ�
B����Ͷ��Na2SO4��Һ�У�������Ӧ2Na+2H2O=2NaOH+H2�����ɷ���ʽ��֪ÿ46g�Ʒ�Ӧ����2g��������Һ��������44g����B�����ϣ�
C����Ͷ���Ȼ����Һ�У��ƺ�ˮ�ķ�Ӧ����ʽΪ��2Na+2H2O=2NaOH+H2�������ɵ��������ƺ��Ȼ�立�Ӧ����Ӧ����ʽΪ��NaOH+NH4Cl=NH3��+NaCl+H2O������������ʽ��ӵ�2Na+2NH4Cl=H2��+2NH3��+2NaCl�����ݷ���ʽ֪��ÿ46g�Ʒ�Ӧ����2g������34g��������Һ��������10g����C�����ϣ�
D���ƺ�ˮ�ķ�Ӧ����ʽΪ��2Na+2H2O=2NaOH+H2�������ɵ��������ƺ�����ͭ��Ӧ����Ӧ����ʽΪ��2NaOH+CuSO4=Na2SO4+Cu��OH��2��������������ʽ��ӵ�2Na+2H2O+CuSO4=H2��+Na2SO4+Cu��OH��2�������ݷ���ʽ֪��ÿ46g�Ʒ�Ӧ����2g������98g������ͭ��������Һ��������2g+98g-46g=54g����D���ϣ�
��ѡD��
���������
�����Ѷȣ�һ��
4������� ������һ��ǿ������������������������ȣ�
��1��O3��KI��Һ��Ӧ���ɵ����ֵ�����______��______���������ʽ��
��2��O3��ˮ���ֽ⣬һ�������£�O3��Ũ�ȼ���һ�������ʱ�䣨t�����±���ʾ����֪��O3����ʼŨ��Ϊ0.0216mol/L��
pH
t/min
T/�� | 3.0 | 4.0 | 5.0 | 6.0
20
301
231
169
58
30
158
108
48
15
50
31
26
15
7
|
��pH�����ܼ���O3�ֽ⣬������O3�ֽ�������õ���______��
����30�桢pH=4.0�����£�O3�ķֽ�����Ϊ______mol/��L?min����
�۾ݱ��еĵݱ���ɣ��Ʋ�O3�����������·ֽ��������������˳��Ϊ______��������ĸ���ţ�
a��?40�桢pH=3.0? b��?10�桢pH=4.0? c��?30�桢pH=7.0
��3��O3���ɳ�����������ԭ����ͼ�����ϡ�����Ƶã�
��ͼ������Ϊ______���A����B��������缫��ӦʽΪ______��
����C��ͨ��O2����A���ĵ缫��ӦʽΪ______��
����C����ͨ��O2��D��E���ֱ��ռ���x?L��y?L���壨��״��������E���ռ���������O3��ռ���������Ϊ______������O3�ķֽ⣩��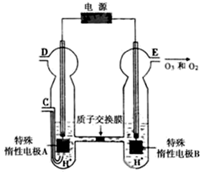
�ο��𰸣���1��O3��KI��Һ��Ӧ���ɵ����ֵ���ֻ��ΪO2��I2���ʴ�Ϊ��O2��I2��
��2����pH������OH-Ũ������pH�����ܼ���O3�ֽ⣬������O3�ֽ�������õ���OH-���ʴ�Ϊ��OH-��?
��v=��ct=0.0108mol/L108min=1.00��10-4mol/��L?min�����ʴ�Ϊ��1.00��10-4��?
���ɱ������ݿ�֪��40��C��pH=3.0ʱ������ʱ����31min��158min֮�䣻
10��C��pH=4.0ʱ������ʱ�䣾231nin��
30��C��pH=7.0ʱ������ʱ�䣼7min����ֽ��������������˳��Ϊb��a��c��
�ʴ�Ϊ��b��a��c��
��3��������ͼ��֪��B������O2��O3��B����Ӧ������Ӧ��������������������Ӧ����AΪ�������缫��ӦΪ2H++2e-�TH2����
�ʴ�Ϊ��A��2H++2e-�TH2����
��C��ͨ��O2��O2������ԭ��Ӧ������������������ˮ���缫��ӦʽΪO2+4H++4e-=2H2O���ʴ�Ϊ��O2+4H++4e-=2H2O��
����C����ͨ��O2��ʵ��Ϊ���ˮ��D��Ϊ���������Ϊx?L��E��Ϊ�����������������Ϊy?L������������ΪZL�����ݵ���ת���غ���
x��2=Z��3��2+��y-Z����2��2�����Z=x-2y������E���ռ���������O3��ռ���������Ϊx-2yy��
�ʴ�Ϊ��x-2yy��
���������
�����Ѷȣ�һ��
5��ѡ���� �������ʵ����Ģ�Na����Na2O����Na2O2����NaOHͶ�뵽�������������ˮ�У��õ������ܣ�����˵����ȷ���ǣ�������
A���١��ڡ��ۡ������ʵ������������
B���ڡ������ʵ����ʵ���Ũ�����
C����������������������ʵ�����������С
D����ȷ���١��ڡ��ۡ���������Һ���ʵ����������Ĵ�С
�ο��𰸣����ȣ������ʵ�����������1mol���Ģ�Na����Na2O����Na2O2����NaOH��Na2O2��Na2O������2molNa�����������������γɵ���Һ�����ʵ����ʵ���Ũ�������Na2O2��ˮ��Ӧ������O2�������൱��Na2O�������ǵȼ۵ģ��������ƺ��������������ʵ����ʵ���Ũ����ȣ������ʵ�����Na������NaOHС���ҽ����ƺ�ˮ��Ӧ����H2�������������ʵ����ʵ���Ũ����Na��NaOH�����õ�������Һ�����ʵ����ʵ���Ũ�ȹ�ϵ��Na2O=Na2O2��Na��NaOH������=�ۣ��٣��ܣ�
��ѡB��
���������
�����Ѷȣ���