1、选择题 下列排列顺序正确的是( )
(1)热稳定性:H2O>HF>H2S?(2)原子半径:Na>Mg>O
(3)酸性:H3PO4>H2SO4>HClO4?(4)氧化性:Cu2+>Mg2+>Na+.
A.(1)(3)
B.(2)(4)
C.(1)(4)
D.(2)(3)
参考答案:(1)因元素的非金属性越强其对应的氢化物越稳定,非金属性:F>O>S,所以热稳定性HF>H2O>H2S,
故(1)错误;
(2)因同周期元素的半径从左至右逐渐减小,Na>Mg,O在Na和Mg的上一周期,半径最小,故(2)正确;
(3)因元素的非金属性越强其对应的最高价氧化物对应的水化物的酸性越强,非金属性:Cl>S>P,酸性:HClO4
>H2SO4>H3PO4,故(3)错误;
(4)金属性:Cu<Mg<Na,所以离子氧化性:Cu2+>Mg2+>Na+,故(4)正确.
故选:B
本题解析:
本题难度:简单
2、选择题 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
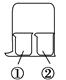
?
| ①中的物质
| ②中的物质
| 预测①的现象
|
A
| 淀粉KI溶液
| 浓硝酸
| 无明显变化
|
B
| 酚酞溶液
| 浓盐酸
| 无明显变化
|
C
| AlCl3溶液
| 浓氨水
| 有白色沉淀
|
D
| 湿润红纸条
| 饱和氯水
| 红纸条褪色
|
?
参考答案:A
本题解析:浓HNO3具有挥发性和强氧化性,所以在①中可能发生反应:6I-+8H++2NO3―=3I2+2NO↑+4H2O,使①中液体变为蓝色。
本题难度:一般
3、选择题 下列元素中,原子半径最小的是
[? ]
A.Si
B.P
C.S
D.Cl
参考答案:D
本题解析:
本题难度:简单
4、选择题 元素在周期表的排列是依照元素的
A.相对原子质量
B.原子序数
C.最高正化合价
D.元素的活泼性
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列实验现象可用同一原理解释的是
A.品红溶液中分别通入SO2和Cl2,品红均褪色
B.溴水分别滴入植物油和裂化汽油中,溴水均褪色
C.鸡蛋白溶液中分别加入NaCl溶液和HgCl2溶液,均有固体析出
D.分别加热盛有NH4Cl和单质碘的试管,管口均有固体凝结
参考答案:B
本题解析:A、SO2通入品红溶液,品红褪色是因为SO2与品红发生非氧化还原反应生成了无色物质,Cl2通入品红溶液,品红褪色是因为Cl2与H2O反应生成了强氧化性的HClO,漂泊了品红,反应原理不同,错误;B、Br2与植物油和裂化汽油都发生了加成反应,反应原理相同,错误;C、NaCl溶液加入鸡蛋白溶液发生了盐析,为物理变化,HgCl2溶液加入鸡蛋白溶液发生了变性,为化学变化,反应原理不同,错误;D、加热NH4Cl分解生成的NH3和HCl在试管口反应,又生成了NH4Cl,为化学变化,加热单质碘,发生升华,在试管口发生凝华,重新得到单质碘,为物理变化,原理不同,错误。
本题难度:一般