1、简答题 I.(1)指出下列实验用品或仪器(已经洗涤干净)使用时的第一步操作:
①蓝色石蕊试纸(检验气体性质)______;
②容量瓶______;
③托盘天平______.
(2)下列有关化学实验操作中“先”与“后”的说法正确的是______(填代号).
A.用排水法收集气体后,先移出导管,后熄灭酒精灯
B.点燃可燃性气体(如CH4、H2、CO等)时,都要先检验气体纯度,后点燃
C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗
D.给试管加热时,先均匀加热,后局部加热
II.实验室利用SO2和一定浓度的NaOH溶液反应制备少量NaHSO3.实验装置如图所示:
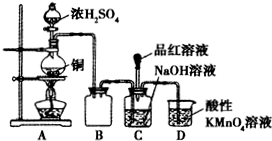
请回答下列问题:
(1)写出圆底烧瓶中发生反应的化学方程式______.
(2)反应结束后发现烧瓶中还有少量的铜片剩余,有人认为还有一定的硫酸剩余,原因是______,在不增加硫酸的情况下,要使剩余铜片溶解,可再加入______固体(填写两种不同类别的物质).
(3)装置B的作用是______,装置D的作用是______.
(4)证明C装置中NaOH溶液全部转化为NaHSO3的实验操作和现象是______.
2、选择题 下列实验用来证明SO2的存在,其中正确的是?
[? ]
①能使品红溶液褪色?②能使湿润的蓝色石蕊试纸变红? ③能使澄清的石灰水变浑浊?
④通入足量的NaOH溶液中,再滴入BaCl2溶液,有白色沉淀生成,该沉淀溶于盐酸
⑤通入溴水能使溴水褪色,再滴入Ba(NO3)2溶液,有白色沉淀生成
A.都能证明?
B.都不能证明?
C.①⑤能证明?
D.只有⑤能证明
3、实验题 某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaOH=________________.
(2)反应Cl2+Na2SO3+2NaOH==2NaCl+Na2SO4+H2O中的还原剂为________________.
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-。
请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
①提出合理假设.
假设1:只存在SO32-;假设2:既不存在SO32-也不存在ClO-;假设3:_____________.
② 设计实验方案,进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂:3moL/LH2SO4、1moL/LNaOH、0.01mol/LKMnO4、淀粉-KI溶液、紫色石蕊试液.
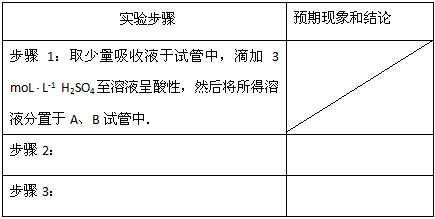
4、选择题 下列几种气体(括号内为溶剂或反应物溶液)按如图所示装置进行实验,不能看到喷泉现象的是
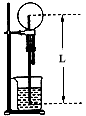
[? ]
A.HCl(H2O)
B.CO2(H2O)
C.SO2(NaOH溶液)
D.NH3(KCl溶液)
5、选择题 能证明SO2具有漂白性的是
[? ]
A.酸性KMnO4溶液中通入SO2气体后,紫色消失
B.显红色的酚酞通入SO2后,红色消失
C.品红溶液中通入SO2后,红色消失
D.溴水中通入SO2后,橙色消失