1��ѡ���� ��CO��H2��O2��ɵĻ������60ml����һ��������ǡ����ȫ��Ӧ�������������101KPa��120��C�¶Կ���������ܶ�Ϊ1.293����ԭ���������H2��ռ���������Ϊ
A��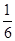
B��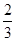
C��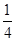
D��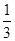
�ο��𰸣�A
�����������ԭ�������CO��H2��O2�����ʵ����ֱ���x��y��z�������ɵ�CO2��ˮ�����ֱ���x��y����������101KPa��120��C�¶Կ���������ܶ�Ϊ1.293�������������ƽ����Է���������29��1.293��37.5������CO2��ˮ���������ʵ���֮���ǣ�37.5��18���£�44��37.5����3�U1������Ϊ0.5x��0.5y��z������y�£�x��y��z����1/6����ѡA��
�����Ѷȣ�һ��
2��ѡ���� �Ƚ�1 mol N2��1 mol CO���������������������ڷ���������ԭ��������������ͬ����
A����
B���٢�
C���٢ڢ�
D���ڢ�
�ο��𰸣�C
���������N2��CO����Է�������Ϊ28������1 mol N2��1 mol CO�Ģ������ڷ���������ԭ������������ͬ��ѡC��
�����Ѷȣ�һ��
3�������� ҽ������������ע��Һ�����˲�����Һ��������ij��������ע��Һÿƿ�����Ϊ500mL��ÿ1000mLע��Һ�к�������5g(�����ǵ���Է�������Ϊ180)��
(1)��������ע��Һ�����ʵ���Ũ���Ƕ���?������������3λС����
(2)ÿ������������������ȫ�����ɷų�15.6kJ��������������ע��500mL����Ũ�ȵ�������Һ�ɲ������������
�ο��𰸣�(1)0.278mol/L
(2)390kJ
���������
�����Ѷȣ�һ��
4��ѡ���� ��NA��ʾ�����ӵ�������ֵ����4(NH4)2SO4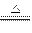 N2+6NH3+3SO2+SO3+7H2O�ķ�Ӧ�У�����NA�����ӷ���ת��ʱ������˵���������(? )
N2+6NH3+3SO2+SO3+7H2O�ķ�Ӧ�У�����NA�����ӷ���ת��ʱ������˵���������(? )
A���� NA����ԭ�ӱ���ԭ
NA����ԭ�ӱ���ԭ
B���� NA����ԭ�ӱ�����
NA����ԭ�ӱ�����
C���� NA�����������������
NA�����������������
D���� NA������立ֽ�
NA������立ֽ�
�ο��𰸣�C
�������������3 mol SO2Ӧ��3��(6-4) mol="6" mol ���ӷ���ת�ƣ�����NA������ת�ƣ�����6��3=NA��x��x= Na�����Է�Ӧ����NA�����ӷ���ת�ƣ�Ӧ��
Na�����Է�Ӧ����NA�����ӷ���ת�ƣ�Ӧ�� NA��SO2�������ɡ�
NA��SO2�������ɡ�
�����Ѷȣ���
5��ѡ���� ��5.1gMg��Al�Ͻ��ܽ��ڹ�����500mL2mol/L�������У�Ȼ�����4mol/LNaOH��Һ����Ҫʹ���ɵij�����࣬��Ӧ���������NaOH��Һ�������
A��200mL
B��250 mL
C��425mL
D��560mL
�ο��𰸣�B
������������ɳ������ʱ����Ϊ�Ȼ��ơ������������������ʵ�����Ϊ1��1�������������������ơ��������������ᣬ�����������ƺ��������ʵ�����Ϊ1��1����4mol/L��V(NaOH)=0.5L��2mol/L��V=0.25L��
������ע��Ԫ���غ�˼������á�
�����Ѷȣ�һ��