微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 将2.8克Fe在一定量稀硝酸中恰好完全溶解后,往溶液中滴加NaOH?溶液立即产生沉淀,滴加至沉淀量最大时,再将所得溶液和沉淀一起加热蒸干,并在空气中灼烧至恒重,所得固体成分和可能的质量为
A.FeO 3.6g???? NaNO3 12.75g
B.Fe2O3 4g???? NaNO2 6.9g
C.Fe3O4 3.87g??? NaNO3 10.25g
D.Fe2O3 4g??? NaNO2 9.8g
选择题 将2.8克Fe在一定量稀硝酸中恰好完全溶解后,往溶液中滴加NaOH?溶液立即产生沉淀,滴加至沉淀量最大时,再将所得溶液和沉淀一起加热蒸干,并在空气中灼 烧至恒重,所得固体成分和可能的质量为
A.FeO 3.6g???? NaNO3 12.75g
B.Fe2O3 4g???? NaNO2 6.9g
C.Fe3O4 3.87g??? NaNO3 10.25g
D.Fe2O3 4g??? NaNO2 9.8g
本题答案:BD
本题解析:分析:根据2.8g Fe与稀硝酸反应可能生成硝酸亚铁或硝酸铁两种情况计算,2.8g Fe的物质的量为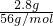 =0.05mol,加入氢氧化钠后蒸干,得到0.05mol氢氧化铁(氢氧化亚铁会被空气氧化)和0.1mol硝酸钠,或硝酸钠0.15mol,最后得到0.025mol氧化铁和0.1mol硝酸钠或0.15mol亚硝酸钠,可分别计算出亚硝酸钠的质量范围.
=0.05mol,加入氢氧化钠后蒸干,得到0.05mol氢氧化铁(氢氧化亚铁会被空气氧化)和0.1mol硝酸钠,或硝酸钠0.15mol,最后得到0.025mol氧化铁和0.1mol硝酸钠或0.15mol亚硝酸钠,可分别计算出亚硝酸钠的质量范围.
解答:如果2.8gFe的物质的量为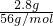 =0.05mol铁全部恰好生成硝酸亚铁,
=0.05mol铁全部恰好生成硝酸亚铁,
则硝酸亚铁物质的量为0.05mol,加入氢氧化钠后蒸干,
得到0.05mol氢氧化铁(氢氧化亚铁会被空气氧化)和0.1mol硝酸钠,
根据元素质量守恒可得加热生成0.025mol氧化铁和0.1mol亚硝酸钠,
质量是:氧化铁0.025mol×160g/mol=4g,亚硝酸钠0.1mol×69g/mol=6.9g
如果恰好生成硝酸铁0.05mol,则氧化铁依然是0.025mol,硝酸钠是0.15mol,
灼烧有氧化铁4g,根据Na元素守恒可得亚硝酸钠0.15mol,质量为0.15mol×69g/mol=10.35g
所以氧化铁质量肯定是4g,亚硝酸钠质量应该在[6.9,10.35]区间内.
故选BD.
点评:本题考查混合物的计算,题目难度较大,注意本题考虑2.8gFe与稀硝酸反应可能生成硝酸亚铁或硝酸铁两种情况计算,利用端值法求解.
本题所属考点:【金属及其化合物】
本题难易程度:【困难】
Let that which is lost be for God. 失去的东西就别想它了. /失去的东西就算献给上帝了.