微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 将一定的NaOH和N www.91exAm.orgaHCO3的混合物放在密闭的容器中加热,充分反应后生成CO2的体积为V1(V1>0).将反应后的固体残渣与过量的稀盐酸反应,又生成CO2的体积为V2(V1、V2均为标准状况的体积).则原混合物中NaOH和NaHCO3的物质的量之比为
A.(V2-V1):(V1+V2)
B.V2:V1
C.V2:(V1+V2)
D.(V1+V2):(V2-V1)
选择题 将一定的NaOH和NaHCO3的混合物放在密闭的容器中加热,充分反应后生成CO2的体积为V1(V1>0).将反应后的固体残渣与过量的稀盐酸反应,又生成CO2的体积为V2(V1、V2均为标准状况的体积).则原混合物中NaOH和NaHCO3的物质的量之比为
A.(V2-V1):(V1+V2)
B.V2:V1
C.V2:(V1+V2)
D.(V1+V2):(V2-V1)
本题答案:A
本题解析:分析:NaOH和NaHCO3的混合物放在密闭的容器中加热,充分反应后生成CO2的体积为V1(V1>0),则剩余固体残渣为Na2CO3,剩余固体残渣与盐酸反应生成CO2的体积为V2,根据碳元素守恒可知碳酸钠的物质的量等于固体残渣与盐酸反应生成CO2的物质的量.根据碳元素守恒可知NaHCO3的物质的量等于两次生成的二氧化碳总的物质的量.令NaOH和NaHCO3的物质的量分别为xmol、ymol,根据钠元素守恒、碳元素守恒列方程计算.
解答:NaOH和NaHCO3的混合物放在密闭的容器中加热,充分反应后生成CO2的体积为V1(V1>0),则剩余固体残渣为
Na2CO3,剩余固体残渣与盐酸反应生成CO2的体积为V2,根据碳元素守恒可知碳酸钠的物质的量等于固体残渣与盐酸反应生成CO2的物质的量.根据碳元素守恒可知NaHCO3的物质的量等于两次生成的二氧化碳总的物质的量.令NaOH和NaHCO3的物质的量分别为xmol、ymol,则:
根据钠元素守恒有x+y=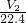 ×2
×2
根据碳元素守恒有y=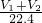
联立解得x=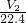 ×2-
×2-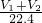 =
=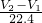
所以原混合物中NaOH和NaHCO3的物质的量之比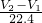 :
: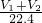 =(V2-V1):(V1+V2).
=(V2-V1):(V1+V2).
故选:A.
点评:考查混合物的计算,难度中等,判断剩余固体残渣为Na2CO3是解题关键,利用常规解法比较 91ExAM.org繁琐,本题采取守恒计算,简化计算.注意守恒思想的运用.
本题所属考点:【金属及其化合物】
本题难易程度:【一般】
People don't resent having nothing nearly as much as too little. 人们埋怨的常常是太少,而不是没有.