微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 常温下,下列有关电解质溶液的叙述正确的是
A.等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7
B.将10?mL?pH=a的盐酸与100?mL?pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13
C.pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知l 91ExaM.orgg?2=0.3)
D.pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性
选择题 常温下,下列有关电解质溶液的叙述正确的是
A.等浓度等体积的强酸与强碱溶液混合后,溶液的pH=7
B.将10?mL?pH=a的盐酸与100?mL?pH=b的Ba(OH)2溶液混合后恰好中和,则a+b=13
C.pH=10的Ba(OH)2溶液和pH=13的NaOH溶液等体积混合后溶液的pH=10.7(已知lg?2=0.3)
D.pH=2的盐酸与pH=12的氨水等体积混合后所得溶液显中性
本题答案:B
本题解析:分析:A.强酸强碱混合溶液的酸碱性不仅取决于酸碱的物质的量还取决于酸和碱的元数;
B.酸碱恰好中和,则盐酸中n(H+)等于氢氧化钡中n(OH-);
C.根据混合溶液中氢氧根离子浓度计算溶液的PH;
D.根据溶液中溶质判断溶液酸碱性.
解答:A.强酸强碱混合溶液的酸碱性不仅取决于酸碱的物质的量还取决于酸和碱的元数,如果n(H+)>n(OH-),溶液呈酸性,如果n(H+)>n(OH-),溶液呈中性,如果n(H+)<n(OH-),溶液呈碱性,故A错误;
B.氯化氢和氢氧化钡都是强电解质,酸碱恰好中和,则盐酸中n(H+)等于氢氧化钡中n(OH-),所以10-a mol/L×0.01L=1014-b mol/L ×0.1L,则a+b=13,故B正确;
C.混合溶液中c(OH-)=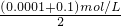 ,c(H+)=
,c(H+)=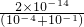 mol/L=2×10-13mol/L,pH=12.7,故C错误;
mol/L=2×10-13mol/L,pH=12.7,故C错误;
D.pH=2的盐酸与pH=12的氨水,氨水的物质的量浓度大于盐酸,所以两种溶液等体积混合后所得溶液显碱性,故D错误;
故选B.
点评:本题考查混合溶液酸碱性的判断及pH的有关计算,根据pH的计算公式及弱电解质电离特点来分析解答,难度中等.
本题所属考点:【电解质溶液】
本题难易程度:【一般】
A good friend is my nearest relation. 好友即至亲.