微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 在100mL含有等物质的量的HBr和H2SO3的溶液中通入0.01mol?Cl2,有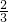 的Br?-转变为Br2(已知Br2能氧化H2SO3).则原溶液中HBr和H2SO3的物质的量浓度为
的Br?-转变为Br2(已知Br2能氧化H2SO3).则原溶液中HBr和H2SO3的物质的量浓度为
A. 0.0075?mol?L-1
B.0.075?mol?L-1
C.0.008?mol?L-1
D.0.08?mol?L-1
选择题 在100mL含有等物质的量的HBr和H2SO3的溶液中通入0.01mol?Cl2,有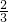 的Br?-转变为Br2(已知Br2能氧化H2SO3).则原溶液中HBr和H2SO3的物质的量浓度为
的Br?-转变为Br2(已知Br2能氧化H2SO3).则原溶液中HBr和H2SO3的物质的量浓度为
A.0.0075?mol?L-1
B.0.075?mol?L-1
C .0.008?mol?L-1
D.0.08?mol?L-1
本题答案:B
本题解析:分析:Br2能氧化H2SO3,则还原性H2SO3>Br-,氯气首先氧化H2SO3为H2SO4,H2SO3反应完毕,然后再氧化Br-,由于Br-部分转变Br2,所以HBr部分被氧化,H2SO3全部被氧化,令原溶液中HBr和H2SO3的浓度为cmol/L,根据电子转移守恒,列方程计算c的值.
解答:Br2能氧化H2SO3,则还原性H2SO3>Br-,氯气首先氧化H2SO3为H2SO4,H2SO3反应完毕,然后再氧化Br-,由于2/3的Br-转变Br2,所以有2/3HBr部分被氧化,H2SO3全部被氧化,令原溶液中HBr和H2SO3的浓度为cmol/L,根据电子转移守恒,则:
0.1L×cmol/L×(6-4)+0.1L×cmol/L×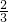 ×1=0.01mol×2,
×1=0.01mol×2,
解得:c=0.075,
故选B.
点评:本题考查氧化还原反应计算,难度中等,根据Br2能氧化H2SO3?判断还原性H2SO3>Br-是关键.
本题所属考点:【氯气的化学性质】
本题难易程度:【困难】
A man can die but once. 人无二死.