微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 标准状况下分别向甲、乙、丙三个容器中加入30.0 mL同浓度的盐酸,再加入不同质量的由两种金属组成的同种合金粉末,测量放出气体的体积。另在甲、乙、丙三个容器中加入30.0 mL与盐酸同浓度的氢氧化钠溶液,再分别加入与上述实验相同质量的同种合金,测量放出气体的体积。所得数据如下表所示:
A.盐酸的物质的量浓度为2 mol・L-1
B.合金可 能由镁与铝组成
C.x=2.016
D.y=2.016
选择题 标准状况下分别向甲、乙、丙三个容器中加入30.0 mL同浓度的盐酸,再加入不同质量的由两种金属组成的同种合金粉末,测量放出气体的体积。另在甲、乙、丙三个容器中加入30.0 mL与盐酸同浓度的氢氧化钠溶液,再分别加入与上述实验相同质量的同种合金,测量放出气体的体积。所得数据如下表所示:
A.盐酸的物质的量浓度为2 mol・L-1
B.合金可能由镁与铝组成
C.x=2.016
D.y=2.016
本题答案:C
本题解析:A:乙、两容器中的盐酸与合金反应产生的氢气的体积相同,可知,丙内的盐酸一定不足,由2HCl~H2↑可知盐酸中溶质为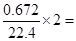 0.06mol,盐酸的浓度为2 mol・L-1,正确
0.06mol,盐酸的浓度为2 mol・L-1,正确
B:甲容器中合金与盐酸反应,合金必定不足,假设合金由镁铝组成,其物质的量分别为x、y,则24x+27y=0.51?? 22.4×(x+3x/2)=0.56,可得x=y=0.01mol;而与NaOH反应中,只有铝可产生氢气,得到的氢气为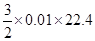 =0.336L,正确
=0.336L,正确
C:乙所对应合金中镁铝的物质的量均为0.03mol,与NaOH溶液反应时,铝粉不足,产生的氢气为: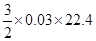 =1.008L,不正确
=1.008L,不正确
D:丙所对应合金中镁铝的物质的量均为0.07mol,与NaOH溶液反应时,铝粉过量,产生的氢气为: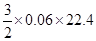 =2.016L,正确
=2.016L,正确
故C选来源:91exam .org项符合题意
本题所属考点:【物质的分离、提纯】
本题难易程度:【困难】
No man is rich enough to buy back his past. 再富有的人也买不回自己的过去.