微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KN03→K20+5Na20+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是
A.生成42.0?L?N2(标准状况)
B.有0.250?mol?KN03被氧化
C.转移电子的物质的量为1.25?mol
D.被氧化的N原子的物质的量为3.75?mol
选择题 汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KN03→K20+5Na20+16N2↑.若氧化产物比还原产物多1.75mol,则下列判断正确的是
A.生成42.0?L?N2(标准状况)
B.有0.250?mol?KN03被氧化
C.转移电子的物质的量为1.25?mol
D.被氧化的N原子的物质的量为3.75?mol
本题答案:C
本题解析:分析:10NaN3+2KN03→K20+5Na20+16N2↑中,N元素由+5价降低为0,反应中共转移10电子,若氧化产物比还原产物多1.75mol,由反应可知,生成16molN2时氧化产物比还原产物多14mol,则该反应生成氮气为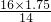 =2mol,以此来解答.
=2mol,以此来解答.
解答:10NaN3+2KN03→K20+5Na20 +16N2↑中,N元素由+5价降低为0,反应中共转移10电子,若氧化产物比还原产物多1.75mol,由反应可知,生成16molN2时氧化产物比还原产物多14mol,则该反应生成氮气为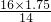 =2mol,
=2mol,
A.生成标况下氮气的体积为2mol×22.4L/mol=44.8L,故A错误;
B.由反应可知,被还原的硝酸钾的物质的量为 =0.25mol,故B错误;
=0.25mol,故B错误;
C.转移电子的物质的量为0.25mol×(5-0)=1.25mol,故C正确;
D.转移2mol电子被氧化的N原子为30mol,则转移1.25mol电子被氧化的N原子的物质的量为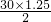 =18.75mol,故D错误;
=18.75mol,故D错误;
故选C.
点评:本题以信息的形式考查氧化还原反应,明确发生的反应及反应中元素的化合价变化即可解答,题目难度不大,注意将N3-作为整体来分析是解答的难点.
本题所属考点:【金属及其化合物】
本题难易程度:【简单】
If you don't want people to know about it, don't do it. 若要人不知,除非己莫为.