微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 用铂电极电解100mL?HNO3与?AgNO3?的混合溶液,通电一段时间后,两极均收集到2.24L气体(标准状况),则原混合溶液中A g+的物质的量浓度为
A.1mol?L-1
B.2?mol?L-1
C.2.5?mol?L-1
D.3?mol?L-1
选择题 用铂电极电解100mL?HNO3与?AgNO3?的混合溶液,通电一段时间后,两极均收集到2.24L气体(标准状况),则原混合溶液中Ag+的物质的量浓度为
A.1mol?L-1
B.2?mol?L-1
C.2.5?mol?L-1
D.3?mol?L-1
本题答案:B
本题解析:分析:铂电极为惰性电极,电解HNO3与AgNO3?的混合溶液,通电一段时间后,两极均收集到2.24L气体(标准状况),阴极发生
2Ag++2e-=2Ag、2H++2e-=H2↑,
阳极发生4OH--4e-=2H2O+O2↑,以此进行计算.
解答:铂电极为惰性电极,电解HNO3与AgNO3?的混合溶液,通电一段时间后,两极均收集到2.24L气体(标准状况),
n(气体)=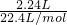 =0.1mol,
=0.1mol,
由阳极发生4OH--4e-=2H2O+O2↑可知,生成0.1molO2转移0.4mol电子,
根据电子守恒可知,阴极转移0.4mol电子,则
2H++2e-=H2↑
?0.2mol 0.1mol
?? 2Ag++2e-=2Ag
0.2mol 0.2mol
即n(Ag+)=0.2mol,
则原混合溶液中Ag+的物质的量浓度为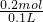 =2mol/L,
=2mol/L,
故选B.
点评:本题考查电解原理及氧化还原反应的计算,明确发生的电极反应及电子守恒是解答本题的关键,注意阴极银离子先放电为解答的易错点,题目难度中等.
本题所属考点:【氧化还原反应】
本题难易程度:【一般】
Don't make mountains out of molehills. 勿把苍蝇说成大象。