| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
某课外小组分别用下图所示装置对原电池和电解池原理进行实验探究【电解池原理】
(3)实验过程中, 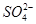 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。 Ⅱ.用图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根( 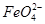 )在溶液中呈紫红色。 )在溶液中呈紫红色。(4)电解过程中,X极区溶液的pH (填“增大”“减小”或“不变”)。 (5)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-  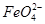 +4H2O和 。 +4H2O和 。 (6)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况下的气体体积),则Y电极(铁电极)质量减少 g。 (7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为: 2K2FeO4+3Zn  F e2O3+ZnO+2K2ZnO2 F e2O3+ZnO+2K2ZnO2该电池正极发生的反应的电极反应为 。 填空题 某课外小组分别用下图所示装置对原电池和电解池原理进行实验探究。 |
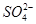 (填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。
(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象有 。 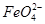 )在溶液中呈紫红色。
)在溶液中呈紫红色。
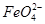 +4H2O和 。
+4H2O和 。  Fe2O3+ZnO+2K2ZnO2
Fe2O3+ZnO+2K2ZnO2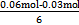 ="0.005" mol;(7)第一步,标化合价看化合价变化:铁的化合价降低3价;第二步,依据得失电子写2
="0.005" mol;(7)第一步,标化合价看化合价变化:铁的化合价降低3价;第二步,依据得失电子写2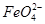 +6e-
+6e- Fe2O3;第三步,依据电荷守恒,结合电解质溶液显碱性配平得电极反应:2
Fe2O3;第三步,依据电荷守恒,结合电解质溶液显碱性配平得电极反应:2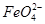 +6e-+5H2O
+6e-+5H2O Fe2O3+10OH-。
Fe2O3+10OH-。 本题所属考点:【电解池原理】
本题难易程度:【困难】
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:Ⅰ.已知在常温常压下:① 2CH3OH.. | ||