|
|
|
近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上【电解池原理】
2016-12-24 00:28:32
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的化学方程式为:KI+3H2O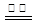 K IO3+3H2↑。下列有关说法不正确的是 ( ) K IO3+3H2↑。下列有关说法不正确的是 ( )
A.电解转移3 mol e-时,理论上可制得KIO3 107 g
B.电解时, 石墨作阳极,不锈钢作阴极
C.电解时的阳极电极反应式:I-?6e-+3H2O = IO3-+6H+
D.电解过程中电解质溶液的pH变小
|
选择题 近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应的化学方程式为:KI+3H2O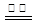 KIO3+3H2↑。下列有关说法不正确的是 ( ) KIO3+3H2↑。下列有关说法不正确的是 ( )
A.电解转移3 mol e-时,理论上可制得KIO3 107 g
B.电解时, 石墨作阳极,不锈钢作阴极
C.电解时的阳极电极反应式:I-?6e-+3H 91Exam.org2O = IO3-+6H+
D.电解过程中电解质溶液的pH变小
|
本题答案:D
本题解析:
试题分析:A、每生成1mol KIO3,则转移6mol电子,所以转移3mol电子时生成0.5mol KIO3,其质量是107g,正确;B、电解时不锈钢作阴极,不能做阳极,否则Fe失去电子而被氧化,正确;C、电解时是I的化合价升高,所以I-在阳极发生氧化反应,生成IO3-,正确;D、电解过程中阳极产生氢离子,而阴极产生氢氧根离子,二者又结合成为水,所以电解质溶液的pH基本不变,错误,答案选D。
考点:考查电解原理的应用
本题所属考点:【电解池原理】
本题难易程度:【一般】
Do what is right, come what may. 不管会发生什么,对的就要去做.