微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (13分)
(1)25℃时,0.1 mol/L的HA溶液中c(H+)/c(OH-)=1010。请回答下列问题:
①HA是 (填“强电解质”或“弱电解质”)。
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是 (填字母)。
A.c(H+)/c(HA) B.c(HA)/(A-) C.c(H+)与c(OH-)的乘积 D.c(OH-)
(2)已知:①CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ・mol-1
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ・mol-1
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 。
(3)下图是利用甲烷燃料电池电解50 mL 2 mol/L的氯化铜溶液的装置示意图:
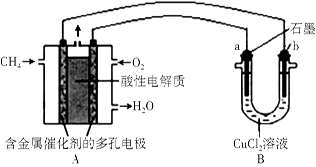
请回答:
① 甲烷燃料电池的负极反应式为 。
② 当线路中有0.6mol电子通过时,B中阳极产物的质量为 g。
填空题 (13分)
(1)25℃时,0.1 mol/L的HA溶液中c(H+)/c(OH-)=1010。请回答下列问题:
①HA是 (填“强电解质”或“弱电解质”)。
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是 (填字母)。
A.c(H+)/c(HA) B.c(HA)/(A-) C.c(H+)与c(OH-)的乘积 D.c(OH-)
(2)已知:①CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ・mol-1
②CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=-247.4 kJ・mol-1
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 。
(3)下图是利用甲烷燃料电池电解50 mL 2 mol/L的氯化铜溶液的装置示意图:

请回答:
① 甲烷燃料电池的负极反应式为 。
② 当线路中有0.6mol电子通过时,B中阳极产物的质量为 g。
本题答案:(1)①弱电解质 ②A、D;
(2)CH&#
本题解析:
试题分析:(1)25℃时,0.1 mol/L的HA溶液中c(H+)/c(OH-)=1010,c(H+)・c(OH-)=101-14,则c (H+)=0.01mol/L<c(HA),所以①HA是弱电解质;②在溶液中存在电离平衡:H 91exam.orgA H++A-,在加水稀释HA溶液的过程中,随着水量的增加c(H+)、c(HA)都减小,电离平衡正向移动,所以c(H+)减小的倍数小于c(HA)减小的倍数,因此c(H+)/c(HA)增大,选项A正确; c(HA)减小的倍数大于 c(A-)减小的倍数,因此c(HA)/(A-)减小,错误;在稀释的过程中,c(H+)减小,但是在水溶液中存在水的电离平衡,由于温度不变,所以c(H+)与c(OH-)的乘积不变,是个常数,选项C错误;由于在水中存在水的电离平衡,c(H+)・c(OH-)="Kw," c(H+)减小,而c(OH-)增大,故选项D正确;(1)①×1-②,整理可得CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H=+659.8 kJ/ mol;(3)① 在甲烷燃料电池中通入燃料甲烷的电极为负极,因为是酸性电解质,所以在电池的负极反应式为CH4-8e-+2H2O=CO2+8H+;② 在B中首先发生反应:CuCl2
H++A-,在加水稀释HA溶液的过程中,随着水量的增加c(H+)、c(HA)都减小,电离平衡正向移动,所以c(H+)减小的倍数小于c(HA)减小的倍数,因此c(H+)/c(HA)增大,选项A正确; c(HA)减小的倍数大于 c(A-)减小的倍数,因此c(HA)/(A-)减小,错误;在稀释的过程中,c(H+)减小,但是在水溶液中存在水的电离平衡,由于温度不变,所以c(H+)与c(OH-)的乘积不变,是个常数,选项C错误;由于在水中存在水的电离平衡,c(H+)・c(OH-)="Kw," c(H+)减小,而c(OH-)增大,故选项D正确;(1)①×1-②,整理可得CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H=+659.8 kJ/ mol;(3)① 在甲烷燃料电池中通入燃料甲烷的电极为负极,因为是酸性电解质,所以在电池的负极反应式为CH4-8e-+2H2O=CO2+8H+;② 在B中首先发生反应:CuCl2 Cu+ Cl2↑。n(CuCl2)= 0.050 L ×2 mol/L=0.1mol,当该物质电解完全时,电子转移0.2mol,在阳极产生氯气0.1mol,后来电解的是水,电解方程式是:2H2O
Cu+ Cl2↑。n(CuCl2)= 0.050 L ×2 mol/L=0.1mol,当该物质电解完全时,电子转移0.2mol,在阳极产生氯气0.1mol,后来电解的是水,电解方程式是:2H2O O2↑+ 2H2↑,由于在整个闭合回路中电子转移数目相等,当线路中有0.6mol电子通过时,电解水转移电子的物质的量是0.4mol,此时产生氧气的物质的量是0.1mol,所以在B中阳极产物的质量为0.1mol×71g/mol+0.1mol×32g/mol=10.3g。
O2↑+ 2H2↑,由于在整个闭合回路中电子转移数目相等,当线路中有0.6mol电子通过时,电解水转移电子的物质的量是0.4mol,此时产生氧气的物质的量是0.1mol,所以在B中阳极产物的质量为0.1mol×71g/mol+0.1mol×32g/mol=10.3g。
考点:考查电解质的强弱的判断、物质稀释过程中微粒的浓度的变化、热化学方程式的书写、原电池和电解池的反应原理及应用的知识。
本题所属考点:【电解池原理】
本题难易程度:【困难】
You can't have everything in this life. 万事如意古来难。