|
|
|
�ò��缫���100mL HNO3 �� AgNO3�Ļ��Һ��ͨ��һ��ʱ�����?������ԭ����
2016-12-24 00:39:31
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
ѡ���� �ò��缫���100mL HNO3 �� AgNO3�Ļ��Һ��ͨ��һ��ʱ����������ռ���2.24 L���壨��״��������ԭ���Һ��Ag+�����ʵ���Ũ��Ϊ
| A��1mol��L��1 | B��2 mol��L��1
| | C��2.5 mol��L��1 | D��3 mol��L��1
|
ѡ���� �ò��缫���100mL HNO3 �� AgNO3�Ļ��Һ��ͨ��һ��ʱ����������ռ���2.24 L���壨��״��������ԭ���Һ��Ag+�����ʵ���Ũ��Ϊ
| A��1mol��L��1 | B��2 mol��L��1
|
| C��2.5 mol��L��1 | D��3 mol��L��1
|
����𰸣�B
���������
������������缫Ϊ���Ե缫�����HNO3��AgNO3�Ļ����Һ��ͨ��һ��ʱ����������ռ���2.24L���壨 ��״������n�����壩=
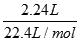
=0.1mol������������4OH--4e-=2H2O+O2����֪������0.1molO2ת��0.4mol���ӣ����ݵ����غ��֪������ת��0.4mol���ӣ�����������2.24L����ת��2x0.1mol=0.2mol���ӣ���2Ag++2e-=2Agת�Ƶ�����Ϊ0.4mol-0.2mol=0.2mol���ӣ��������ӵ����ʵ���Ϊ0.2mol��ԭ�����Һ��Ag+�����ʵ���Ũ��Ϊ
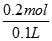
=2mol/L����ΪB.
���㣺���ԭ��
�����������㣺������ԭ����
�������׳̶ȣ���һ�㡿
No man is indispensable. û��һ�����Dz���ȱ�ٵġ�/����˭����Ҳת��
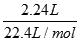 =0.1mol������������4OH--4e-=2H2O+O2����֪������0.1molO2ת��0.4mol���ӣ����ݵ����غ��֪������ת��0.4mol���ӣ�����������2.24L����ת��2x0.1mol=0.2mol���ӣ���2Ag++2e-=2Agת�Ƶ�����Ϊ0.4mol-0.2mol=0.2mol���ӣ��������ӵ����ʵ���Ϊ0.2mol��ԭ�����Һ��Ag+�����ʵ���Ũ��Ϊ
=0.1mol������������4OH--4e-=2H2O+O2����֪������0.1molO2ת��0.4mol���ӣ����ݵ����غ��֪������ת��0.4mol���ӣ�����������2.24L����ת��2x0.1mol=0.2mol���ӣ���2Ag++2e-=2Agת�Ƶ�����Ϊ0.4mol-0.2mol=0.2mol���ӣ��������ӵ����ʵ���Ϊ0.2mol��ԭ�����Һ��Ag+�����ʵ���Ũ��Ϊ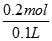 =2mol/L����ΪB.
=2mol/L����ΪB.