微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 熔融盐燃料电池具有较高的发电效率,因而受到重视。某燃料电池以熔融的K2CO3(其中不含O2-和HCO )为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电 极反应式为:2C4H10+26CO
)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电 极反应式为:2C4H10+26CO -52e-===34CO2+10H2O。
-52e-===34CO2+10H2O。
试回答下列问题:
(1)该燃料电池的化学反应方程式为______________________________________________;
(2)正极电极反应式为____________________________________________。
(3)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此,必须在通入的空气中加入一种物质,加入的物质是________,它来自____________。
(4)某学生想用该燃料电池和如图所示装置来电解饱和食盐水:
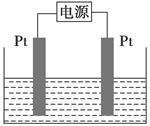
①写出反应的离子方程式_______________________________________。
②将湿润的淀粉KI试纸放在该装置附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5∶1,且生成两种酸。该反应的化学方程式为_______________________________________________________________。
③若电解后得到200 mL 3.25 mol・L-1 NaOH溶液,则消耗C4H10的体积在标准状况下为________mL。
填空题 熔融盐燃料电池具有较高的发电效率,因而受到重视。某燃料电池以熔融的K2CO3(其中不含O2-和HCO )为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电极反应式为:2C4H10+26CO
)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电极反应式为:2C4H10+26CO -52e-===34CO2+10H2O。
-52e-===34CO2+10H2O。
试回答下列问题:
(1)该燃料电池的化学反应方程式为______________________________________________;
(2)正极电极反应式为____________________________________________。
(3)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此,必须在通入的空气中加入一种物质,加入的物质是________,它来自____________。
(4)某学生想用该燃料电池和如图所示装置来电解饱和食盐水:

①写出反应的离子方程式_______________________________________。
②将湿润的淀粉KI试纸放在该装置附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化。若反应的Cl2和I2的物质的量之比为5∶1,且生成两种酸。该反应的化学方程式为_______________________________________________________________。
③若电解后得到200 mL 3.25 mol・L-1 NaOH溶液,则消耗C4H10的体积在标准状况下为______ __mL。
本题答案:(1)2C4H10+13O2===8CO2+10H2O本题解析:
试题分析:(1)该燃料电池的反应实质是丁烷与氧气反应生成二氧化碳、水,所以总反应的化学方程式为2C4H10+13O2===8CO2+10H2O
(2)用总反应方程式减去负极反应方程式可得正极反应方程式为13O2+26CO2+52e-===26CO
(3)该反应的中有水生成,所以在空气中应充入二氧化碳,以保证碳酸钾电解质的稳定性;二氧化碳来自于电池的负极;
(4)①电解饱和食盐水得到氯气、氢气、氢氧化钠,反应的离子方程式为2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
②氯气将生成的I2氧化,得到两种酸,反应的Cl2和I2的物质的量之比为5∶1,说明1个Cl原子得电子的数目是1个I原子失去电子数目的1/5,所以Cl的化合价由0价降为-1价,则I的化合价由0价升高为+5价,结合溶液中的水判断该两种酸是HCl和H HIO3,化学方程式为5Cl2+I2+6H2O===10HCl+2HIO3
③电解后得到200 mL 3.25 mol・L-1 NaOH溶液,氢氧化钠的物质的量 是0.65mol,转移电子的物质的量是0.65mol,根据2C4H10+26CO -52e-===34CO2+10H2O,得需要丁烷的物质的量是0.025mol,标准状况下的体积是0.025mol×22.4L/mol=0.56L=560mL。
-52e-===34CO2+10H2O,得需要丁烷的物质的量是0.025mol,标准状况下的体积是0.025mol×22.4L/mol=0.56L=560mL。
考点:考查电化学反应原理的应用与计算
本题所属考点:【电解池原理】
本题难易程度:【困难】
Ignorance of the law excuses no man. 不知法不能使任何人免罪.