微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分)电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。
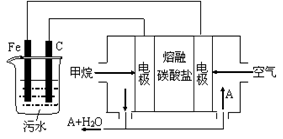
(1 )实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的__________(填序号)。
a.H2SO4
b.BaSO4
c.Na2SO4
d.NaOH
e.CH3CH2OH
(2)电解池阳极发生两个电极反应,反应式分别是:①__________;②4OH――4e―= O2↑+2H2O;
(3)电极反应①和②的生成物发生反应得到Fe(OH)3的离子方程式是________________;
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂。已知负极的电极反应是CH4 + 4CO32― ― 8e―="=" 5CO2 + 2H2O。
①正极的电极反应是___________________;
②为了使该电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A参加循环(见上图)。A物质的化学式是__________;
(5)实验过程中,若阴极产生44.8 L(标况)气体,则燃料电池消耗CH4(标况)_____L。
填空题 (12分)电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6. 91EXAm.org0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。

(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的__________(填序号)。
a.H2SO4
b.BaSO4
c.Na2SO4
d.NaOH
e.CH3CH2OH
(2)电解池阳极发生两个电极反应,反应式分别是:①__________;②4OH――4e―= O2↑+2H2O;
(3)电极反应①和②的生成物发生反应得到Fe(OH)3的离子方程式是________________;
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂。已知负极的电极反应是CH4 + 4CO32― ― 8e―="=" 5CO2 + 2H2O。
①正极的电极反应是___________________;
②为了使该电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A参加循环(见上图)。A物质的化学式是__________;
(5)实验过程中,若阴极产生44.8 L(标况)气体,则燃料电池消耗CH4(标况)_____L。
本题答案:(1)C(2分) (2)Fe ― 2e―="=" Fe2+(
本题解析:
试题分析:(1)要保持保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀时,因此加入能使溶液导电能力增强的电解质必须是可溶于水的、显中性的盐,答案选c;
(2)燃料电池中通入空气的电极是正极,通入甲烷的电极是负极。铁与正极相连作阳极,活泼金属电极做电解池的阳极时,电极本身失去电子,电极反应式为Fe-2e-=Fe2+;
(3)阳极铁失去电子转化为亚铁离子,亚铁离子具有还原性,能被氧气氧化生成铁离子,铁离子与氢氧根离子结合生成氢氧化铁红褐色沉淀,反应的离子方程式可表示为4Fe2++10H2O+O2=4Fe(OH)3↓+8H+;
(4)①燃料电池中,正极得到电子发生还原反应,即一定是氧气得电子的过程。由于电解质是熔融碳酸盐,因此正极电极反应为O2+2CO2+4e-=2CO32-;
②负极甲烷失去电子转化为CO2,而正极需要消耗CO2,所以可以循环利用的物质是二氧化碳;
(5)阴极电极反应为2H++2e-=H2↑,即44.8L(标准状况)气体是氢气,物质的量是2mol,转移电子的物质的量为4mol。根据电池的负极电极反应CH4+4CO32--8e-=5CO2+2H2O可知当转移4mol电子时,消耗CH40.5mol,在标准状况下的体积V=0.5mol×22.4L/mol=11.2L。
考点:考查电化学原理的应用
本题所属考点:【电解池原理】
本题难易程度:【困难】
It takes two to speak truth-one to speak and another to hear. 说真话要有两个人――一个说,一个听。