|
|
|
用惰性电极电解一定量的硫酸铜溶液,当转移0.4 mol电子时,阴极?【电解池原理】
2016-12-24 01:05:54
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 ; 用惰性电极电解一定量的硫酸铜溶液,当转移0.4 mol电子时,阴极开始产生气体,继续电解又转移0.2 mol电子时停止电解。下列说法正确的是
A.电解过程中,溶液的pH不断增大
B.当转移0.4 mol 电子时,电解生成的铜为12.8 g
C.阴极反应式为2H2O+4e-=4H++O2↑
D.整个过程中产生的H2与O2的体积比为2:1
|
选择题 用惰性电极电解一定量的硫酸铜溶液,当转移0.4 mol电子时,阴极开始产生气体,继续电解又转移0.2 mol电子时停止电解。下列说法正确的是
A.电解过程中,溶液的pH不断增大
B.当转移0.4 mol 电子时,电解生成的铜为12.8 g
C.阴极反应式为2H2O+4e-=4H++O2↑
D.整个过程中产生的H2与O2的体积比为2:1
|
本题答案:B
本题解析:
试题分析:A.电解过程分两阶段,第一阶段电解硫酸铜溶液后溶液呈酸性,第二阶段,实际上在电解水,酸性增强,错误;B.第一阶段2CuSO4 +2H2O
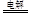
2Cu↓+O2↑+2H2SO4转移4e-,当转移0.4 mol 电子时,电解生成的铜为12.8 g ,正确;C.整个电解过程分两阶段,阴极反应式为Cu+2e-=Cu、2H++2e-=H2↑,错误;D.第一阶段2CuSO4 +2H2O
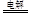
2Cu↓+O2↑+2H2SO4转移4e-
0.1 0.4
第二阶段:2H2O
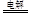
2H2↑+O2↑转移4e-
0.1 0.05 0.1 整个过程中产生的氢气和氧气的体积比为2:3,错误;选B。
考点:考查电解原理的应用。
本题所属考点:【电解池原理】
本题难易程度:【一般】
There is no mistake so great as that of being always right. 最大的错误莫过于总是自信正确。
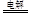 2Cu↓+O2↑+2H2SO4转移4e-,当转移0.4 mol 电子时,电解生成的铜为12.8 g ,正确;C.整个电解过程分两阶段,阴极反应式为Cu+2e-=Cu、2H++2e-=H2↑,错误;D.第一阶段2CuSO4 +2H2O
2Cu↓+O2↑+2H2SO4转移4e-,当转移0.4 mol 电子时,电解生成的铜为12.8 g ,正确;C.整个电解过程分两阶段,阴极反应式为Cu+2e-=Cu、2H++2e-=H2↑,错误;D.第一阶段2CuSO4 +2H2O 2Cu↓+O2↑+2H2SO4转移4e-
2Cu↓+O2↑+2H2SO4转移4e- 2H2↑+O2↑转移4e-
2H2↑+O2↑转移4e-