微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (10分)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,总反应如下:2 CH3CHO+H2O CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH
实验室中,以一定浓度的乙醛―Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示。
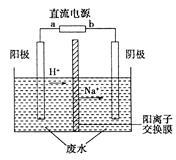
(1)若以锌锰碱性电池为直流电源,该电池总反应式为:Zn+2MnO2+2H2O===2MnO(OH)+Zn(OH)2。该电池的a电极的电极反应式为:_____________________________________________。
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。电极反应式如下:
阳极:①4OH--4e-===O2↑+2H2O。
②_______________________________________________。
阴极:①__________________________________________。
②CH3CHO+2e-+2H2O===CH3CH2OH+2OH-。
(3)电解过程中,某时刻测定了阳极区溶液中各组分的物质的量,其中Na2SO4与CH3COOH的物质的量相同。此时刻下列关于阳极区溶液中各微粒浓度关系的说法正确的是 (填序号)。
a.c(Na+)=2c(CH3COOH)+2c(CH3COO-)
b.c(Na+)+c(H+)=c(SO42-)+c(CH3COO-)+c(OH-)
c.c(Na+)>c(CH3COOH)>c(CH3COO-)>c(OH-)
(4)已知:乙醛、乙醇的沸点分别为20.8 ℃、78.4 ℃。从电解后阴极区的溶液中分离出乙醇粗品的方法是 。
填空题 (10分)最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,总反应如下:2CH3CHO+H2O CH3CH2OH+CH3COOH
CH3CH2OH+CH3COOH
实验室中,以一定浓度的乙醛―Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如图所示。

(1)若以锌锰碱性电池为直流电源,该电池总反应式为:Zn+2MnO2+2H2O===2MnO(OH)+Zn(OH)2。该电池的a电极的电极反应式为:_____________________________________________。
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。电极反应式如下:
阳极:①4OH--4e-===O2↑+2H2O。
②_______________________________________________。
阴极:①__________________________________________。
②CH3CHO+2e-+2H2O===CH3CH2OH+2OH-。
(3)电解过程中,某时刻测定了阳极区溶液中各组分的物质的量,其中Na2SO4与CH3COOH的物质的量相同。此时刻下列关于阳极区溶液中各微粒浓度关系的说法正确的是 (填序号)。
a.c(Na+)=2c(CH3COOH)+2c(CH3COO-)
b.c(Na+)+c(H+)=c(SO42-)+c(CH3COO-)+c(OH-)
c.c(Na+)>c(CH3COOH)>c(CH3COO-)>c(OH-)
(4)已知:乙醛、乙醇的沸点分别为20.8 ℃、78.4 ℃。从电解后阴极区的溶液中分离出乙醇粗品的方法是 。
本题答案: (1) 2MnO2+2H2O+2e-=2MnO(OH)+2
本题解析:
试题分析:(1)a电极与电解池的阳极相连,这说明a是正极。根据电池总反应式Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2可正极是二氧化锰得到电子,则该电池的a电极的电极反应式为2MnO2+2H2O+2e-=2MnO(OH)+2OH-。
(2)电解池中阳极失去电子,除了氢氧根放电 外,乙醛失去电子转化为乙酸,反应的电极反应式外CH3CHO-2e-+H2O=CH3COOH+2H+;阴极得到电子,除了乙醛得到电子转化为乙醇以外,溶液中的氢离子也得到电子转化为氢气,电极反应式为2H++2e-=H2↑。
(3)电解过程中,某时刻测定了阳极区溶液中各组分的物质的量,其中Na2SO4与CH3COOH的物质的量相同。此时刻下列关于阳极区溶液中各微粒浓度关系的说法正确的是 (填序号)。
a.根据物料守恒可知c(Na+)=2c(CH3COOH)+2c(CH3COO-),a正确;b.根据电荷守恒c(Na+)+c(H+)=2c(SO42-)+c(CH3COO-)+c(OH-)可知c(Na+)+c(H+)=c(SO42-)+c(CH3COO-)+c(OH-)是错误的,b不正确;c.醋酸是一元弱酸,电离常数小,则溶液中c(Na+)>c(CH3COOH)>c(CH3COO-)>c(OH-),c正确,答案选ac。
(4)已知:乙醛、乙醇的沸点分别为20.8 ℃、78.4 ℃,由于二者互溶,所以从电解后阴极区的溶液中分离出乙醇粗品的方法是蒸馏。
考点:考查电化学原理的应用、溶液中离子浓度比较以及物质的分离与提纯
本题所属考点:【电解池原理】
本题难易程度:【困难】
It is not the lofty sails but the unseen wind that moves the ship. 推动船的不是高大的帆,而是无形的风。