微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (16分)金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以钛铁矿(主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质)为主要原料冶炼金属钛,其生产的工艺流程图如下:
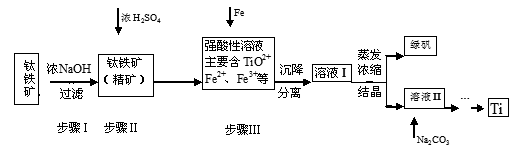
已知:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O
(1)步骤I中发生反应的离子方程式: 、 。
(2)已知:TiO2+易水解,只能存在于强酸性溶液中。
25 ℃时,难溶电解质溶解度(s)与pH关系如图,TiO(OH)2溶度积Ksp=1×10-29

①步骤Ⅲ加入铁屑原因是 。
②TiO2+水解的离子方程式为 。向溶液II中加入Na2CO3粉末的作用是 。
当溶液pH接近 时,TiO(OH)2已沉淀完全。
(3)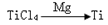 反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
| TiCl4
| Mg
| MgCl2
| Ti
|
熔点/℃
| -25.0
| 648.8
| 714
| 1667
|
沸点/℃
| 136.4
| 1090
| 1412
| 328 7
|
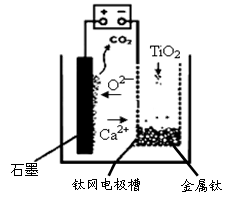
(4)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。写出阳极上所发生的反应式: 。
填空题 (16分)金属钛(Ti)性能优越,被称为继铁、铝之后的“第三金属”。工业上以钛铁矿(主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质)为主要原料冶炼金属钛,其生产的工艺流程图如下:

已知:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O
(1)步骤I中发生反应的离子方程式: 、 。
(2)已知:TiO2+易水解,只能存在于强酸性溶液中。
25 ℃时,难溶电解质溶解度(s)与pH关系如图,TiO(OH)2溶度积Ksp=1×10-29

①步骤Ⅲ加入铁屑原因是 。
②TiO2+水解的离子方程式为 。向溶液II中加入Na2CO3粉末的作用是 。
当溶液pH接近 时,TiO(OH)2已沉淀完全。
(3)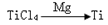 反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
反应后得到Mg、MgCl2、Ti的混合物,可采用真空蒸馏的方法分离得到Ti,依据下表信息,需加热的温度略高于 ℃即可。
| TiCl4
| Mg
| MgCl2
| Ti
|
熔点/℃
| -25.0
| 648.8
| 714
| 1667
|
沸点/℃
| 136.4
| 1090
| 1412
| 3287
|
(4)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。写出阳极上所发生的反应式: 。

本题答案:(1)Al2O3+2OH-=2AlO2-+H2O (2分);
本题解析:
试题分析:钛铁矿(主要成分FeTiO3,含FeO、Al2O3、SiO2等杂质)当向其中加入NaOH溶液时,Al2O3、SiO2会发生反应,离子方程式是:Al2O3+2OH-=2AlO2-+H2O;SiO2+2OH-=SiO32-+H2O;(2)①得到的精矿中含有FeTiO3,FeO来源:91考试网 91ExAm.org,然后向其中加入浓硫酸,发生反应:2H2SO4(浓)+ FeTiO3=TiOSO4 + FeSO4 + 2H2O;4H2SO4(浓)+2FeO=Fe2(SO4)3+SO2↑+4H2O,得到含有H+、Fe2+、Fe3+、TiO2+的溶液,步骤Ⅲ加入铁屑原因会发生反应:2Fe3++Fe=3Fe2+;防止Fe3+与TiO同时生成沉淀;② TiO2+水解的离子方程式为TiO2++2H2O=TiO(OH)2+2H+;向溶液II中加入Na2CO3粉末的作用是消耗溶液中的H+,调节溶液pH值;根据图像可知,当溶液pH接近3时,TiO(OH)2已沉淀完全;(3)TiCl4在隔绝空气时加入Mg发生置换反应产生Ti、MgCl2,同时还有过量的金属Mg,根据混合物中Mg、Ti、MgCl2的熔沸点关系可知当加热的温度略高于1412℃时,Mg、MgCl2变为气体逸出;而Ti则恰好刚刚熔化,因此可以达到分离提纯的目的。(4)由于用惰性电极石墨电极作阳极,所以电解质中的阴离子在阳极放电,该电极的电极式是:2O2―-4e-=O2↑;C+O2=CO2;或写为:C+2O2―-4e-=CO2↑。
考点:考查铁、铝、硅的化合物的性质、盐的水解、反应条件的控制、离子方程式的书写、电解原理在物质制取中的应用的知识。
本题所属考点:【电解池原理】
本题难易程度:【困难】
Wisdom in the mind is better than money in the hand. 头脑里的知识比手中的金钱更有用.