|
|
|
用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循?【电解池原理】
2016-12-24 23:26:41
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH同时得到某种副产物,其原理如图所示(电极材料为石墨)。下列说法不正确的是
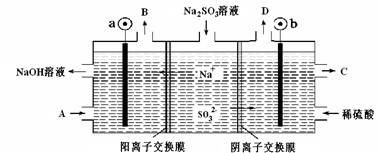
A.b电极上的主反应是 SO32--2e-+H2O===SO42-+2H+
B.若D是混合气体,则可能含有SO2、O2等成分
C.a 电极发生还原反应,当有1mol Na+ 通过阳离子交换膜时,a极生成11.2L气体
D.A溶液是稀NaOH溶液,作用是增强溶液的导电性;C是较浓的硫酸溶液
|
选择题 用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH同时得到某种副产物,其原理如图所示(电极材料为石墨)。下列说法不正确的是

A.b电极上的主反应是 SO32--2e-+H2O===SO42-+2H+
B.若D是混合气体,则可能含有SO2、O2等成分
C.a 电极发生还原反应,当有1mol Na+通过阳离子交换膜时,a极生成11.2L气体
D.A溶液是稀NaOH溶液,作用是增强溶液的导电性;C是较浓的硫酸溶液
|
本题答案:C
本题解析:
试题分析:A、根据装置图中亚硫酸根离子的移动方向判断,b极是阳极,则b极发生氧化反应,亚硫酸根离子失去电子,生成硫酸,正确;B、因为b极是阳极,发生氧化反应,则可能发生氢氧根离子的失去电子的氧化反应,生成氧气,同时通入的稀硫酸也可能与亚硫酸根离子反应生成二氧化硫,所以若D是混合气体,则可能含有SO2、O2等成分,正确;C、a电极是阴极,发生还原反应,氢离子得到电子生成氢气,当有1mol Na+通过阳离子交换膜时 ,说明有1mol氢离子放电生成0.5mol氢气,但未指明标准状况,所以a极气体的体积不一定是11.2L,错误;D、因为a极是氢离子放电,造成阴极区的氢氧根离子浓度增大,与移动过来的氢氧根离子形成氢氧化钠,所以A是稀氢氧化钠溶液,增强溶液的导电性;同理阳极通入的是稀硫酸,亚硫酸根离子被氧化生成硫酸,则出来的物质C是相对较浓的硫酸,正确,答案选C。
考点:考查电化学反应原理的应用
本题所属考点:【电解池原理】
本题难易程度:【困难】
Never hope for too much. 不要期望太多.