微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 【化学-选修2 化学与技术】
下图是传统的工业生产金属铝的基本流程图。结合铝生产的流程图回答下列问题:
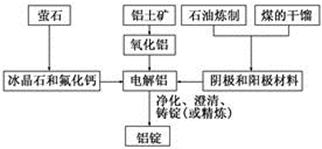
(1)工业冶炼金属铝用的是铝土矿,铝土矿的主要成分是________(填化学式)。石油炼制和煤的干馏产品__________(填物质名称)作电解铝的阴极和阳极材料。
(2)在金属铝的冶炼中加入冰晶石和氟化钙的目的是________
(3)在冶炼过程中,阳极材料需要定期进行更换,原因是氧化铝溶解并和部分冰晶石发生反应生成Al2OF62-,写出该反应的离子方程式________________。若电解的总反应为2Al2O3+3C 3CO2+4Al,则阳极的电极反应式为_______________。
3CO2+4Al,则阳极的电极反应式为_______________。
(4)冰晶石能在碱性溶液中分解,写出冰晶石与足量NaOH溶液反应生成两种钠盐的化学方程式______________。
(5)已知生产1mol铝消耗的电能为1.8x106J,9g铝制饮料罐可回收能量为0.2kJ,则铝制饮料罐的热回收效率η=_____________。(热回收效率= 回收能量/生产耗能 x100%)
填空题 【化学-选修2 化学与技术】
下图是传统的工业生产金属铝的基本流程图。结合铝生产的流程图回答下列问题:

(1)工业冶炼金属铝用的是铝土矿,铝土矿的主要成分是________(填化学式)。石油炼制和煤的干馏产品__________(填物质名称)作电解铝的阴极和阳极材料。
(2)在金属铝的冶炼中加入冰晶石和氟化钙的目的是________
(3)在冶炼过程中,阳极材料需要定期进行更换,原因是氧化铝溶解并和部分冰晶石发生反应生成Al2OF62-,写出该反应的离子方程式________________。若电解的总反应为2Al2O3+3C 3CO2+4Al,则阳极的电极反应式为_______________。
3CO2+4Al,则阳极的电极反应式为_______________。
(4)冰晶石能在碱性溶液中分解,写出冰晶石与足量NaOH 溶液反应生成两种钠盐的化学方程式______________。
(5)已知生产1mol铝消耗的电能为1.8x106J,9g铝制饮料罐可回收能量为0.2kJ,则铝制饮料罐的热回收效率η=_____________。(热回收效率= 回收能量/生产耗能 x100%)
本题答案:(1)Al2O3;碳素材料;(2)降低Al2O3的熔点,减少
本题解析:
试题分析:(1)铝土矿的成分是Al2O3、Fe2O3、SiO2,主要成分是Al2O3;电解时的阴阳级材料是能导电的,一般是金属和石墨,而石油炼制和煤的干馏中不含金属,因此石油炼制和煤的干馏产品是碳素材料作电解铝的阴极好阳极材料;(2)金属铝冶炼是电解熔融状态下氧化铝,因为氧化铝的熔点非常高,消耗大量的电能,因此加入冰晶石和氟化钙可以降低氧化铝的熔点,减少电能的消耗;(3)冰晶石Na3[AlF6],氧化铝和冰晶石生成Al2OF62-和F-,根据反应前后原子个数守恒,Al2OF62-系数为3,则AlF63-系数4,化学反应方程式:Al2O3+4AlF63-===3Al2OF62-+6F-;电解时阳极是失电子,化合价升高,根据总反应C的化合价由0→+4,C参与了正极反应,冰晶石在整个电解过程中降低氧化铝的熔点,反应前后质量不变,阳极电极反应:C+2 Al2OF62-+12F--4e-===CO2↑+4 AlF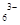 ;(4)(4)冰晶石Na3[AlF6]与足量NaOH溶液反应生成两种钠盐,根据元素守恒和原子个数守恒,Na作阳离子,Al作为阴离子AlO2-,F作为阴离子F-,反应的化学反应方程式:
;(4)(4)冰晶石Na3[AlF6]与足量NaOH溶液反应生成两种钠盐,根据元素守恒和原子个数守恒,Na作阳离子,Al作为阴离子AlO2-,F作为阴离子F-,反应的化学反应方程式: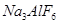 +4NaOH===6NaF+NaAlO2+2H2O;(5)9gAl的物质的量=
+4NaOH===6NaF+NaAlO2+2H2O;(5)9gAl的物质的量=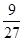 mol=
mol= mol,生产
mol,生产 mol铝消耗的电能为
mol铝消耗的电能为 ×1.8×106=6×105J,则热回收效率η=
×1.8×106=6×105J,则热回收效率η=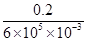 ×100%=0.033%。
×100%=0.033%。
考点:考查化学反应方程式的书写、材料的成分、化学计算等相关知识。
本题所属考点:【电解池原理】
本题难易程度:【困难】
Do not do to others what you would not have them do to you. 己所不欲,勿施于人。