|
|
|
关于甲、乙装置的下列叙述中正确的是<img src="http://www.9【电解池原理】
2016-12-24 23:31:10
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 关于甲、乙装置的下列叙述中正确的是
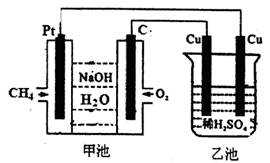
A.甲池中通甲烷的极是负极,溶液中Na+向Pt电极移动
B.C电极的电极反应为:O2+4e-+4H+==2H2O
C.乙池中的总反应为:Cu+H2SO4 H2 H2 +CuSO4 +CuSO4
D.反应过程中,甲、乙装置中溶液的pH都逐渐减小
|
选择题 关于甲、乙装置的下列叙述中正确的是

A.甲池中通甲烷的极是负极,溶液中Na+向Pt电极移动
B.C电极的电极反应为:O2+4e-+4H+==2H2O
C.乙池中的总反应为:Cu+H2SO4 H2 H2 +CuSO4 +CuSO4
D.反应过程中,甲、乙装置中溶液的pH都逐渐减小
|
本题答案:C
本题解析:
试题分析:A.甲池中通燃料甲烷的极是负极,根据同种电荷相互排斥,异种电荷相互吸引的原则,溶液中阳离子Na+向负电荷较多的正极C电极移动,错误;B.在燃料电池的正极C电极上发生还原反应,由于是碱性环境,所以正极上的电极反应为:O2+4e-+2H2O ==4OH-,错误;C.乙池中与电源的正极C连接的电极为阳极,发生反应:Cu-2e-=Cu2+,与电源的负极连接的Cu电极为阴极,发生反应:2H++2e-=H2↑,所以总反应为:Cu+H2SO4

H2↑+CuSO4,正确;D.反应过程中,甲装置的总方程式是:CH4+O2+2NaOH=Na2CO3+3H2O,不断消耗Na OH溶液,同时产生水,因此c(NaOH)碱性,溶液的pH逐渐减小,而对于乙装置,反应的总方程式是:Cu+H2SO4

H2↑+CuSO4,溶液的酸性逐渐减弱,所以溶液的pH逐渐增大,错误。
考点:考查原电池、电解池的反应原理及应用的知识。
本题所属考点:【电解池原理】
本题难易程度:【困难】
They have rights who dare defend them. 敢于保卫权利的人就能拥有权利。
 H2↑+CuSO4,正确;D.反应过程中,甲装置的总方程式是:CH4+O2+2NaOH=Na2CO3+3H2O,不断消耗Na OH溶液,同时产生水,因此c(NaOH)碱性,溶液的pH逐渐减小,而对于乙装置,反应的总方程式是:Cu+H2SO4
H2↑+CuSO4,正确;D.反应过程中,甲装置的总方程式是:CH4+O2+2NaOH=Na2CO3+3H2O,不断消耗Na OH溶液,同时产生水,因此c(NaOH)碱性,溶液的pH逐渐减小,而对于乙装置,反应的总方程式是:Cu+H2SO4 H2↑+CuSO4,溶液的酸性逐渐减弱,所以溶液的pH逐渐增大,错误。
H2↑+CuSO4,溶液的酸性逐渐减弱,所以溶液的pH逐渐增大,错误。