|
|
|
高铁酸盐在能源环保领域有广泛用途。用镍(Ni),铁做电极电解浓【电解池原理】
2016-12-24 23:34:16
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 高铁酸盐在能源环保领域有广泛用途。用镍(Ni),铁做电极电解浓氢氧化钠溶液制备Na2FeO4的装置如图,说法合理的是
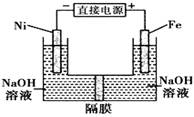
A.镍是阳极,电极反应4OH--4e-=2H2O+O2↑
B.电解时电流方向:负极→镍电极→溶液→铁电极→正极
C.若隔膜是阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低,阴极区pH升高,撤去隔膜后与原溶液比较pH降 低(假设电解前后体积变化忽略不计)
|
选择题 高铁酸盐在能源环保领域有广泛用途。用镍(Ni),铁做电极电解浓氢氧化钠溶液制备Na2FeO4的装置如图,说法合理的是

A.镍是阳极,电极反应4OH--4e-=2H2O+O2↑
B.电解时电流方向:负极→镍电极→溶液→铁电极→正极
C.若隔膜是阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低,阴极区pH升高,撤去隔膜后与原溶液比较pH降低(假设电解前后体积变化忽略不计)
|
本题答案:D
本题解析:
试题分析:A、根据电解池的工作原理,跟电源正极相连的一极称为阳极,跟电源负极相连的称为阴极,镍是阴极,电极反应式:2H++2e-=H2↑,错误;B、电流方向是从正极出发经外电路流向负极,错误;C、根据电解池的工作原理电解液中阴离子向阳极移动,向右移动,错误;D、阴极电极反应式:2H2O+2e-=H2↑+2OH-,pH增大,阳极上反应式:Fe +8OH--6e-=FeO42-+4H2O,消耗氢氧根pH减小,撤去隔膜,总反应式:2H2O+Fe+2OH-

FeO42-+3H2↑,消耗了氢氧根离子,pH降低,正确。
考点:考查电解池的工作原理、pH与酸碱行的关系。
本题所属考点:【电解池原理】
本题难易程度:【困难】
The same man never crossed the same river twice. 旧地重来景已非。
 FeO42-+3H2↑,消耗了氢氧根离子,pH降低,正确。
FeO42-+3H2↑,消耗了氢氧根离子,pH降低,正确。