微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (12分)(1)由氢气和氧气反应生成1 mol水蒸气放热241.8kJ,写出该反应的热化学方程式: 。若1g水蒸气转化成液态水放热2.5kJ,则氢气的燃烧热为△H= kJ/mol。
(2)近年来已经研制出甲烷(CH4)燃料电池,该电池的电解质溶液为H2SO4溶液,
写出该电池负极的电极反应式:_____________________________。
该电池总反应式:_____________________________。
(3)用惰性电极电解AgNO3溶液,写出该电解反应的化学方程式 ;若在阳极收集到 0.32 g O2,中和电解生成的酸需0.4 mol・L-1NaOH溶液 mL
填空题 (12分)(1)由氢气和氧气反应生成1 mol水蒸气放热241.8kJ,写出该反应的热化学方程式: 。若1g水蒸气转化成液态水放热2.5kJ,则氢气的燃烧热为△H= kJ/mol。
(2)近年来已经研制出甲烷(CH4)燃料电池,该电池的电解质溶液为H2SO4溶液,
写出该电池负极的电极反应式:_____________________________。
该电池总反应式:_____________________________。
(3)用惰性电极电解AgNO3溶液,写出该电解反应的化学方程式 ;若在阳极收集到 0.32 g O2,中和电解生成的酸需0.4 mol・L-1NaOH溶液 mL
本题答案:(1)makesmallpic(this,600,1800);' src=) ;18g水蒸气转化成液态水放热2.5kJ×18,由氢气和氧气反应生成1 mol液态水放热241.8kJ+2.5kJ×18,所以氢气的燃烧热为△H=―286.8kJ/mol;(2)甲烷燃料电池,电解质溶液为H2SO4溶液,总反应即甲烷燃烧的方程式
;18g水蒸气转化成液态水放热2.5kJ×18,由氢气和氧气反应生成1 mol液态水放热241.8kJ+2.5kJ×18,所以氢气的燃烧热为△H=―286.8kJ/mol;(2)甲烷燃料电池,电解质溶液为H2SO4溶液,总反应即甲烷燃烧的方程式 ,负极反应为甲烷失电子,发生氧化反应,反应式为
,负极反应为甲烷失电子,发生氧化反应,反应式为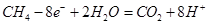 。(3)电解AgNO3溶液,阳极OH―发生氧化反应生成氧气,阴极Ag+的电子发生还原反应生成银单质,所以总反应为
。(3)电解AgNO3溶液,阳极OH―发生氧化反应生成氧气,阴极Ag+的电子发生还原反应生成银单质,所以总反应为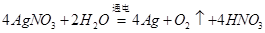 ;得到0.01mol gO2,生成硝酸0.04mol,所以消耗氢氧化钠0.04mol,根据
;得到0.01mol gO2,生成硝酸0.04mol,所以消耗氢氧化钠0.04mol,根据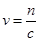 ,消耗氢氧化钠溶液100mL
,消耗氢氧化钠溶液100mL
考点:本题考查热化学方程式、燃料电池、电解原理。
本题所属考点:【原电池原理】
本题难易程度:【一般】
Fools learn nothing from wise men,but wise men learn much form fools. 傻瓜从聪明人那儿什么也学不到,而聪明人却能从傻瓜那儿学到不少东西.