微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (共10分)常温下,如果取0.1 mol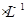 HA溶液与0.1mol
HA溶液与0.1mol 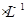 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因:____(用离了方程式表示)。
(2)混合溶液中由水电离出的c(OH-)=____
(3)求出混合溶液中下列算式的精确计算结果(填具体数值):
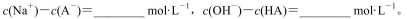
(4)己知NH4A 溶液为中性,又知HA溶液加到Na2 CO3溶液中有气体放出,试推断(NH3)2CO3溶液的pH_____7(填“>”、“<”或“=”);
填空题 (共10分)常温下,如果取0.1 mol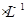 HA溶液与0.1mol
HA溶液与0.1mol 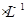 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因:____(用离了方程式表示)。
(2)混合溶液中由水电离出的c(OH-)=____
(3)求出混合溶液中下列算式的精确计算结果(填具体数值):
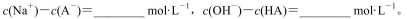
(4)己知NH4A 溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH3)2CO3溶液的pH_____7(填“>”、“<”或“=”);
本题答案:(每空2分,共10分)
(1)A-+H2O![]() 本题解析:
本题解析:
(1)等物质的量的一元酸和一元碱恰好 91Exam.org反应生成盐和水,生成的盐溶液呈碱性说明该酸是弱酸, 生成的盐能水解导致溶液中OH-浓度大于H+浓度,溶液的pH值大于7,水解的离子方程式为A-+H2O HA+OH-
HA+OH-
(2)该盐含有弱根离子能促进水的电离,溶液显碱性,溶液中的OH-都是由水电离所得,该溶液的PH=8,POH=6,则混合溶液中由水电离出的c( OH-)= 1.0×10-6mol・L-1
(3)由电荷守恒可知,c(Na+)-c(A-)=c(OH-)-c(H+)=10-6-10-8=9.9×10-7mol/L;0.1mol/L HA溶液与0.1mol/L NaOH溶液等体积混合生成NaA溶液;测得混合溶液的pH=8,c(H+)=10-8mol/L;溶液显碱性,说明A-离子水解,溶液中存在质子守恒:c(OH-)=c(H+)+c(HA),则c(OH-)-c(HA)=c(H+)=10-8mol/L;
(4)将HA溶液加到Na2CO3溶液中有气体放出,说明HA的酸性比碳酸的强,NH4A溶液为中性,说明相同条件下,氨水和HA的电离程度相同,所以(NH4)2CO3中铵根离子的水解程度小于碳酸根离子的水解程度,所以溶液的pH>7。
考点:考查盐类的水解,酸碱混合时的守恒关系及有关PH的计算等知识。
本题所属考点:【盐类水解的原理】
本题难易程度:【一般】
None so old that he hopes not for a year of life. 老寿星也不会嫌寿长.