微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (15分)海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
成分
| Na+
| K+
| Ca2+
| Mg2+
| Cl-
| SO42-
| HCO3-
|
含量/mg?L-1
| 9360
| 83
| 160
| 1100
| 16000
| 1200
| 118
|
(1)海水显弱碱性的原因是(用离子方程式表示): ,该海水中Ca2+的物质的量浓度为__________mol/L 。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图所示。其中阴(阳)离子交换膜只允许阴(阳)离子通过,电极均为惰性电极。

① 开始时阳极的电极反应式为 。
② 电解一段时间, 极(填“阴”或“阳”)会产生水垢,其成份为 (填化学式)。
③ 淡水的出口为a、b、c中的__________出口。
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如图所示:
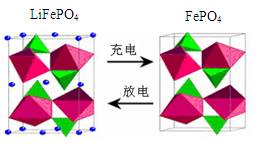
该电池电解质为能传导 Li+的固体材料。
上面左图中的小黑点表示 (填粒子符号),充电时该电极反应式为 。
(4)利用海洋资源可获得MnO2 。MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾。该制备过程中消耗相同条件下氯气和空气的体积比为 (空气中氧气的体积分数按20%计)。
填空题 (15分)海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
成分
| Na+
| K+
| Ca2+
| Mg2+
| Cl-
| SO42-
| HCO3-
|
含量/mg?L-1
| 9360
| 83
| 160
| 1100
| 16000
| 1200
| 118
|
(1)海水显弱碱性的原因是(用离子方程式表示): ,该海水中Ca2+的物质的量浓度为__________mol/L 。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如下图所示。其中阴(阳)离子交换膜只允许阴(阳)离子通过,电极均为惰性电极。

① 开始时阳极的电极反应式为 。
② 电解一段时间, 极(填“阴”或“阳”)会产生水垢,其成份为 (填化学式)。
③ 淡水的出口为a、b、c中的__________出口。
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如图所示:

该电池电解质为能传导 Li+的固体材料。
上面左图中的小黑点表示 (填粒子符号),充电时该电极反应式为 。
(4)利用海洋资源可获得MnO2 。MnO2可用来制备高锰酸钾:将MnO2与KOH混合后在空气中加热熔融,得到绿色的锰酸钾(K2MnO4),再利用氯气将锰酸钾氧化成高锰酸钾。该制备过程中消耗相同条件下氯气和空气的体积比为 (空气中氧气的体积分数按20%计)。
本题答案:(1)HCO3-+H2O海水中含有碳酸氢根离子,水解显碱性,离子方程式为HCO3-+H2O<img onload='if(this.width>600)makesmallpic(this,600,1800);' src=) H2CO3+OH-。根据表中数据可知该海水中Ca2+的物质的量浓度为
H2CO3+OH-。根据表中数据可知该海水中Ca2+的物质的量浓度为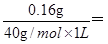 4×10-3 mol/L。
4×10-3 mol/L。
(2)①电解池中阳极失去电子,发生氧化反应,因此开始时是海水中的氯离子放电,则开始时阳极的电极反应式为2Cl--2e-=Cl2↑。
②由于阴极是氢离子放电生成氢气,从而在阴极产生氢氧根,氢氧根与镁离子结合生成CaCO3和Mg(OH)2。产生的氢氧根还能与碳酸氢根反应生成碳酸根,因此还有碳酸钙沉淀产生,则电解一段时间,阴极会产生水垢,其成份为CaCO3和Mg(OH)2。
③在外加电流的作用下海水中的阴阳离子分别通过阴离子交换膜和阳离子交换膜移动,从而使1个间隔室的海水被淡化,而相邻间隔室的海水被浓缩,则根据装置图可知a和c是被浓缩的海水,则淡水的出口为b口。
(3)海水中锂元素储量非常丰富,从海水中提取锂的研究极具潜力。锂是制造化学电源的重要原料,如LiFePO4电池某电极的工作原理如右图所示:该电池电解质为能传导 Li+的固体材料。这说明锂是该电池的负极,失去电子,阳离子Li+向正极移动。则根据示意图可知左图中的小黑点表示Li+。充电是放电的逆反应,即该电极是阳极,阳极失去电子,则充电时该电极的反应式为LiFePO4-e-=FePO4+Li+ 。
(4)假设反应中得到1mol高锰酸钾,则由锰酸钾转化为高锰酸钾时锰元素的化合价从+6价升高到+7价,失去1个电子,则需要氯气0.5mol。得到1mol锰酸钾,其中锰元素的化合价从+4价升高到+6价,失去2个电子。氧气在反应中得到4个电子,则根据电子得失守恒可知需要氧气是0.5mol,因此氯气与氧气的体积之比是1:1。又因为氧气在空气中的体积份数是0.2,因此氯气与空气的体积比为1:5。
考点:考查海水资源的综合利用、氧化还原反应以及电化学原理的应用等
本题所属考点:【盐类水解的原理】
本题难易程度:【困难】
No one is a fool always, every one sometimes. 没有终生的傻瓜,也没有终生不当傻瓜的人.