|
|
|
常温下,用0.1000mol・L-1NaOH溶液滴定20.00mL 0.1000mol・L-1CH【水的电离平衡】
2016-12-25 17:30:59
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
选择题 常温下,用0.1000mol・L-1NaOH溶液滴定20.00mL 0.1000mol・L-1CH3COOH溶液,滴定曲线如右图。下列说法正确的是
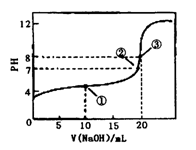
A.点①所示溶液中:[CH3COO-]+[OH-]=[CH3COOH] +[H+]
B.点②所示溶液中:[Na+]=[CH3COOH]+[CH3COO-]
C.点③所示溶液中:[Na+]>[OH-]>[CH3COO-]>[H+]
D.滴定过程中可能出现:[CH3COOH]>[CH3COO-]>
| [H+]>[Na+」>[OH-]
选择题 常温下,用0.1000mol・L-1NaOH溶液滴定20.00mL 0.1000mol・L-1CH3COOH溶液,滴定曲线如右图。下列说法正确的是

A.点①所示溶液中:[CH3COO-]+[OH-]=[CH3COOH] +[H+]
B.点②所示溶液中:[Na+]=[CH3COOH]+[CH3COO-]
C.点③所示溶液中:[Na+]>[OH-]>[CH3COO-]>[H+]
D.滴定过程中可能出现:[CH3COOH]>[CH3COO-]>
|
[H+]>[Na+」>[OH-]
本题答案:D
本题解析:A 错误,应遵循电荷守恒,[CH3COO-]+[OH-]=[Na+]+[H+]
B 错误,点②所示溶液PH=7,显中性,[Na+]=[CH3COO-]
C 错误,点③所示溶液中:[Na+]>[CH3COO-]>[OH-]>[H+]
D 正确。在CH3COOH溶液中开始滴入很少量的NaOH溶液时出现此种情况。
本题所属考点:【水的电离平衡】
本题难易程度:【一般】
Two wrongs do not make a right. 两个错误,加不出一个正确. /用错误改正不了错误.