微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
计算题 (6分)(1)常温下100mL0.05 mol・L-1的氢氧化钡溶液中滴加硫酸钠溶液,当两者恰好完全反应时,测得溶液的pH为12。则加入硫酸钠溶液的体积是____________ ml。(溶液混合时体积的变化不计,下同)
(2)常温下,若100体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的PH(用a表示)与强碱的PH(用b表示)之间应满足的关系是 &来源:www.91exam.org#160; 。
(3)已知100℃ KW=1×10-12 ,0.1mol/LNaOH溶液,由水电离出的OH-物质的量的浓度为 ,PH= 。
计算题 (6分)(1)常温下100mL0.05 mol・L-1的氢氧化钡溶液中滴加硫酸钠溶液,当两者恰好完全反应时,测得溶液的pH为12。则加入硫酸钠溶液的体积是____________ ml。(溶液混合时体积的变化不计,下同)
(2)常温下,若100体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的PH(用a表示)与强碱的PH(用b表示)之间应满足的关系是 。
(3)已知100℃ KW=1×10-12 ,0.1mol/LNaOH溶液,由水电离出的OH-物质的量的浓度为 ,PH= 。
本题答案:(6分)(1)900。(2) a+b="16" 。(3) 1
本题解析:(1)由题意知,原溶液的pH=13,加入硫酸钠溶液后pH=12,即相当于稀释为原先溶液体积的10倍,所以加入溶液体积为900ml
(2)代入公式:a+b=14+lg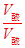 =16
=16
(3)0.1mol/LNaOH溶液中,H+全部来自于水的电离;所以c(H+)=10-12/0.1=10-11,所以由水电离出的OH-物质的量的浓度为1.0×10-11mol/L,pH即为11
本题所属考点:【水的电离平衡】
本题难易程度:【困难】
Like author, like book. 书如其人。